Mit zwei Proteinen zur Hightech-Faser
Materialforscher aus Jena verbinden zwei natürliche Proteine zu Nano-Fasern für Medizin und Technik.
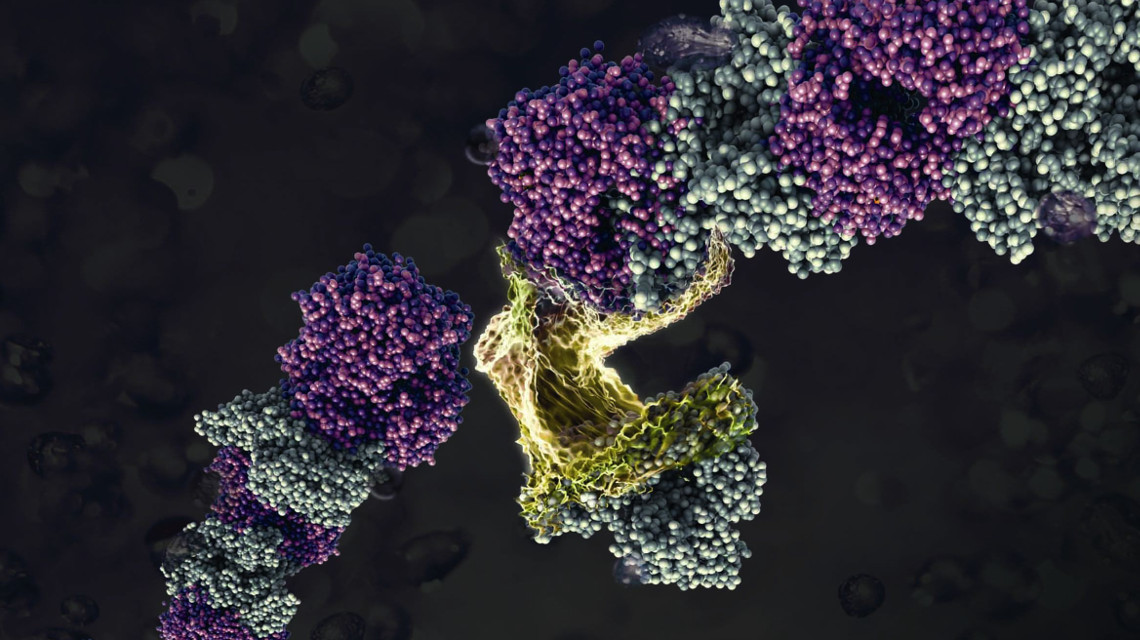
Proteine machen etwa die Hälfte des Trockengewichts aller lebenden Zellen aus. So häufig, wie die umgangssprachlich oft als Eiweiße bezeichneten Moleküle sind, so vielseitig sind sie auch. Sie bilden Strukturen mit teils erstaunlichen Eigenschaften, von extrem hoher Festigkeit bis zu antibakterieller Wirksamkeit. Materialforschern der Friedrich-Schiller-Universität Jena ist es nun gelungen, zwei Sorten von Proteinen kontrolliert zu einer Nanofaser zu vereinigen. So könnten künftig funktionelle Naturstoffe für medizinische, elektronische und weitere Anwendungen entstehen, berichten die Wissenschaftler im Fachjournal „ACS Nano“.
Natürlicher Prozess schwer nachzubauen
„Die Natur baut diese Nanomaterialien, die einen Durchmesser von etwa einem Tausendstel eines menschlichen Haares aufweisen, durch Selbstorganisationsprozesse“, erläutert der Jenaer Materialforscher Klaus Jandt. Der Nachbau dieser Proteinfasern hat sich bislang jedoch als schwierig erwiesen. Für die natürlichen Proteine Fibrinogen und Fibronektin war das Jandt und seiner Gruppe bereits gelungen. Sogar ob sich die Fasern linear oder verzweigt entwickeln, konnte die Jenaer steuern.
Jetzt sind sie einen Schritt weitergegangen und haben einen Prozess entwickelt, der Proteinnanofasern aus unterschiedlichen Proteinen erzeugt. Das Ziel der Materialforscher: Später einmal sollen so Fasern mit vorgegebenen Eigenschaften entstehen, die dann Bausteine in Biosensoren, Wirkstofftransportpartikeln, optischen Sonden oder Knochenzementen bilden.
Machbarkeit nachgewiesen
Den Machbarkeitsnachweis erbrachten die Wissenschaftler mit dem Protein Albumin, das für den osmotischen Druck im Blut verantwortlich ist, und dem Protein Hämoglobin, das zum Sauerstofftransport im Blut dient. Zunächst lösten die Jenaer die Proteine in Ethanol und erwärmten dann die Lösung auf 65 Grad Celsius. Natürliche Mechanismen sorgten anschließend dafür, dass sich die unterschiedlichen Proteine zu einer gemeinsamen Faser verbanden.
Wie das funktioniert, enträtselten die Jenaer gemeinsam mit Wissenschaftlern des Leibniz-Instituts für Photonische Technologien in Jena. Sie wiesen mittels Spektroskopie nach, dass die aus Aminosäuren aufgebauten Proteine sich dort verbunden hatten, wo die Abfolge der Aminosäuren bei beiden Proteinen große Ähnlichkeiten aufwies. Angetrieben wird der selbstorganisierte Prozess von elektrostatischen und hydrophoben Wechselwirkungen.
Künftige Anwendungsmöglichkeiten
Die Jenaer Forscher sind zuversichtlich, dass dieser neue Selbstorganisationsansatz erfolgreich auf andere Proteine übertragen werden kann, wenn diese in Teilen die gleichen Aminosäuresequenzen aufweisen. Jandt ist zuversichtlich: „Dadurch ist das Tor aufgestoßen für eine ganz neue Generation von funktionellen Materialien für die Medizintechnik, die Nanoelektronik, Sensorik oder die Optik, die auf natürlichen Stoffen und Bauprinzipien basieren."
bl