CO2-Recycling für den Klimaschutz und die industrielle Transformation
Fossile Rohstoffe müssen dringend durch erneuerbare Alternativen ersetzt werden, um die Klimaschutzziele zu erreichen und die Wirtschaft krisenfest und wettbewerbsfähig aufzustellen.
Bis 2050 will Europa gemäß dem European Green Deal der erste treibhausgasneutrale und nachhaltige Kontinent werden. Deutschland hat sich mit dem Klimaschutzgesetz noch ambitioniertere Ziele gesetzt und will bis 2045 klimaneutral werden.
Treibhausgas-Emissionen müssen drastisch reduziert werden, um unsere Ökosysteme zu schützen und dem Klimawandel entgegenzutreten. Von besonderer Bedeutung ist es, die Rohstoffversorgung mit Kohlenstoff auf erneuerbare Quellen umzustellen (Defossilisierung) und eine Kreislaufwirtschaft mit ressourceneffizienten Wertschöpfungsnetzwerken voranzutreiben.
Das gilt auch für die chemische Industrie, deren Produkte auf dem Element Kohlenstoff basieren, das bislang überwiegend aus Erdöl oder Erdgas gewonnen wird. Das Verwenden fossiler Rohstoffe verursacht CO2-Emissionen während der Produktion von Chemikalien oder Kunststoffen und der energetischen Verwertung nach dem Gebrauch der Produkte. Weltweit beansprucht die Chemikalienproduktion rund 300 Millionen Tonnen an fossilem Kohlenstoff. Gleichzeitig wurden in Deutschland nach Zahlen des Umweltbundesamtes im Jahr 2021 rund 167 Millionen Tonnen Kohlenstoffdioxid bei Industrieprozessen ausgestoßen, davon 5,5 Millionen Tonnen von der chemischen Industrie. Bis heute werden anfallende Abfallströme der Industrie, wie zum Beispiel Abgase, größtenteils nicht wiederverwertet und tragen zu einem linearen Wirtschaftssystem bei.
Um Arzneimittel, Kunststoffe oder Baustoffe in Zukunft klimaneutral aus „erneuerbarem Kohlenstoff“ herstellen zu können, braucht es neue Lösungen. Im Mittelpunkt einer solchen Strategie stehen geschlossene Kreisläufe – und die Nutzung des emittierten Kohlenstoffs als Rohstoff für die industrielle Produktion.
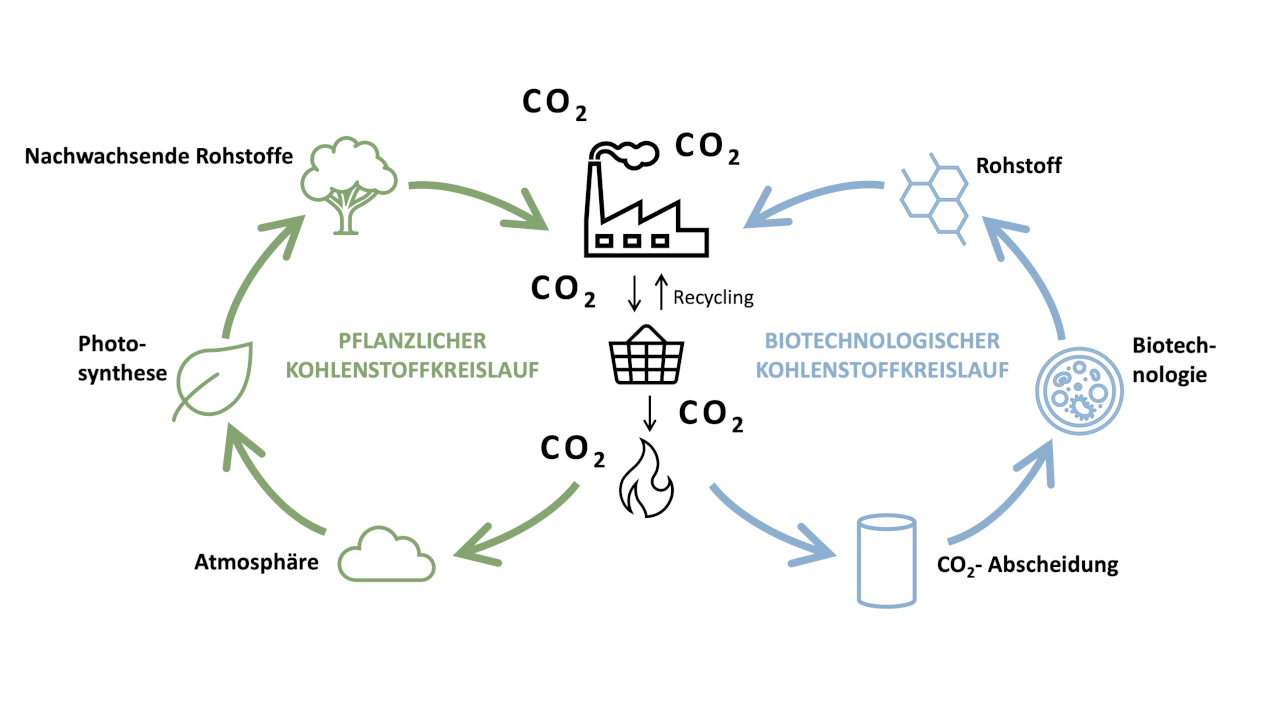
Das Ziel: Kohlenstoff im Kreislauf führen
Ein Ziel der Bioökonomie ist es, in sich geschlossene Kreislaufsysteme aufzubauen, in denen möglichst wenige Substanzen aus dem Kreislauf abgegeben werden. Das wird erreicht, indem nachwachsende Rohstoffe effizient genutzt und Abfallströme in den Kreislauf reintegriert werden.
In der Natur zirkulieren biologische Ressourcen in Stoffkreisläufen. Die Nutzung und Neubildung stehen im Gleichgewicht. Die natürlichen Stoffkreisläufe werden von Lebewesen und insbesondere den Mikroorganismen maßgeblich vorangetrieben. Der Stoffwechsel der Lebewesen ist Teil des natürlichen Kohlenstoffkreislaufs. Ein Teil des Kohlenstoffs wird durch die Atmung und Zersetzung von organischem Material freigesetzt und sammelt sich in der Atmosphäre. Ein anderer Teil kann langfristig in Sediment gebunden werden, so etwa in nassen Moorböden. Die Pflanzen binden das CO2 wiederum in ihrer Biomasse. Entspricht das emittierte Kohlenstoffvolumen demjenigen, das in neuer Biomasse gebunden wird, ist die Kohlenstoffbilanz ausgeglichen, also klimaneutral.
Durch die Nutzung von Erdöl, Erdgas und Kohle wird über Millionen Jahre in fossilen Ressourcen gebundener Kohlenstoff schnell und in großen Mengen als CO2 freigesetzt. Die übermäßigen Mengen CO2, die in die Atmosphäre abgegeben werden, bringen die Kohlenstoffbilanz aus dem Gleichgewicht und führen zum Treibhauseffekt.
CO2-Nutzungs- und Speichertechnologien, sogenannte carbon capture and utilization/storage (CCU/CCS) Technologien, können dem Treibhauseffekt entgegenwirken. CCS-Projekte zielen auf eine langfristige Speicherung des Kohlenstoffs in geologischen Formationen ab. CCU hingegen bietet die Chance, fossilen Kohlenstoff aus industriellen Prozessen wiederzuverwenden und somit den Kohlenstoffkreislauf durch industrielle Verfahren zu schließen (technisch-industrieller Kohlenstoffkreislauf). In (bio)chemischen Umwandlungsprozessen können mit CO2 beispielsweise synthetische Kraftstoffe oder Grundstoffe für die chemische Industrie sowie für die Baubranche hergestellt werden. Das CO2 für eine nachhaltige Nutzung kann im Prinzip aus zwei unterschiedlichen Quellen stammen – zum einen aus industriellen Prozessen, wenn diese Emissionen nicht vermieden werden können (sogenannte prozessbedingte Emissionen) und zum anderen lässt sich mit vergleichsweise höherem Aufwand auch das CO2 aus der Atmosphäre nutzen.
Express-Erklärvideo: CO2 als Rohstoff
Auf dem Weg in eine kreislaufbasierte Bioökonomie können biotechnologische CCU-Verfahren Potenziale eröffnen, um fossile Rohstoffe in Produktionsprozessen zu ersetzen. Hierbei wird CO2 als Rohstoff in den Wertschöpfungskreislauf eingebunden. Indem Mikroorganismen das Gas verwerten, kann energieeffizientes Recycling beziehungsweise Upcycling durch Biotechnologie ermöglicht werden. Biotechnologisches CO2-Recycling zur Produktion von Chemikalien stellt eine Möglichkeit dar, die negativen Folgen der Ressourcenverknappung in der chemischen Industrie abzuschwächen und die Chemikalienherstellung vom Verbrauch fossiler Ressourcen zu entkoppeln.
Seite 2 von 7
Drei Wege vom kohlenstoffhaltigen Gas zum biobasierten Produkt
Ein wichtiges Ziel der Bioökonomie ist es, durch biobasierte Innovationen Treibhausgas-Emissionen zu verringern und CO2 als Rohstoffquelle zu nutzen. Doch wie kann das Gasmolekül mit nur einem C-Atom zu einem nachhaltigen Produkt umgewandelt werden? Kohlenstoffdioxid ist ein reaktionsträges Molekül, das heißt es muss Energie aufgewendet werden, um daraus Biomasse und organische Moleküle für Kraftstoffe, Chemikalien oder Kunststoffe herstellen zu können.
Es gibt drei biobasierte Wege für die Verwertung von CO2:
Photosynthese: In der Natur wird CO2 aus der Atmosphäre mithilfe von Sonnenenergie gebunden und in Biomasse umgesetzt. Dieser Stoffwechselprozess ist als Photosynthese bekannt und in Pflanzen, Algen und einigen Bakterien zu finden. Mittels Sonnenlicht wird Wasser gespalten und CO2 in Zucker und Sauerstoff umgewandelt. Um Pflanzen und Makroalgen für die biologischen CO2-Verwertung zu verwenden, muss ein hoher Flächen- und Ressourcenbedarf für den Anbau gedeckt werden. Im Gegensatz dazu beansprucht die Kultivierung von Mikroorganismen weniger Platz. Photosynthetisch aktive Mikroalgen und Cyanobakterien können CO2 über die Photosynthese reduzieren und in Biomasse umsetzen. Die Organismen können in technischen Anlagen sowohl atmosphärisches CO2 als auch CO2-haltige Abfallströme wie Abgase verwerten. Als Produkte entstehen Biomasse, Fettsäuren, Vitamine, Farbstoffe sowie weitere hochwertige Metaboliten (siehe Kapitel 5).
Gasfermentation: Ein weiterer biotechnologischer Ansatz zum CO2-Recycling basiert auf nicht-photosynthetisch aktiven Mikroorganismen. Über bestimmte Stoffwechselwege sind CO2 und Kohlenstoffmonoxid (CO) für sie zugänglich. Auf Basis dieser Kohlenstoffquellen können die Bakterien sowohl einfache Produkte (etwa Methan, Ethanol) als auch komplexe Produkte (etwa Polymere) bilden. Diese können als Ausgangsprodukte für Chemikalien, Lebensmittel, Kosmetik, Verpackungsmaterial und Biokraftstoffe genutzt werden (siehe Kapitel 3).
Elektrobiosynthese stellt einen weiteren biotechnologischen Ansatz dar, Kohlenstoffdioxid in hochwertige Produkte umzuwandeln. Durch die Kombination von biotechnologischen und elektrochemischen Verfahrensschritten können komplexe Chemikalien hergestellt werden (siehe Kapitel 4).
Seite 3 von 7
Gasfermentation: Mikroorganismen mit CO2 füttern
Beim biotechnologischen Verfahren der Gasfermentation werden Mikroorganismen eingesetzt, die mithilfe ihres Stoffwechsels aus CO2 oder CO höherwertige Produkte herstellen. Als Ausgangsstoff und Energiequelle werden synthesegasähnliche Stoffe genutzt. Hauptbestandteile von Synthesegas sind CO und Wasserstoff (H2). Zu den Ausgangsstoffen für die Gasfermentation zählen auch industrielle Abgase, die sich vor allem in der Stahl-, Zement- und Chemieindustrie finden. CO2 aus der Umgebungsluft kann (noch) nicht für die direkte Verarbeitung genutzt werden, da die Konzentration mit 0,04 % zu gering ist.
Bei der mikrobiellen Gasfermentation werden anaerob (unter Sauerstoffausschluss) oder aerob (mit Sauerstoff) lebende Bakterienstämme genutzt, die CO2/CO als Substrat für das Herstellen spezifischer Produkte nutzen können. Dabei wird Kohlenstoff über den mikrobiellen Stoffwechsel fixiert, unter Energieaufwand reduziert und weiterverarbeitet.
Bei allen Gasfermentationsverfahren muss H2 oder CO als Energieträger zugeführt werden. Die Fermentation findet in Bioreaktoren statt, in welche das kohlenstoffhaltige Gas geführt wird. In industriellem Maßstab werden Blasensäulen- oder Gaslift-Reaktoren verwendet.
Die natürlichen Produkte der Gasfermentation sind z.B. Ethanol und Essigsäure. Diese finden in der chemischen und pharmazeutischen Industrie sowie Lebensmittel-, Automobil-, Getränke- und Kosmetikbranche Anwendung. Ethanol gilt als wichtiger Bestandteil von Biokraftstoff, Essigsäure ist eine wichtige Basis-Chemikalie um Acetatester, Essigsäureanhydrid, Vinylacetatmonomer (VAM) und gereinigte Terephthalsäure (PTA) herzustellen. Welche Produkte von den Mikroorganismen hergestellt werden, hängt von der Kohlenstoffquelle und den Stoffwechselwegen der Bakterien ab.
Gasfermentation mit anaeroben Bakterien
Für die mikrobielle Gasfermentation können anaerobe Bakterien eingesetzt werden. Häufig verwendete Bakterienarten gehören zum Stamm der Acetogenen. Sie verstoffwechseln CO2 zu dem Intermediat Acetyl-CoA, welches dann in Acetat (Essigsäure) und Ethanol umgewandelt wird. Es können auch Butanol, Hexanol sowie biologische Rohstoffe wie Lactat, Butyrat, Hexanoat, 2,3-Butandiol, Isopropanol oder Aceton hergestellt werden. Der Stoffwechselweg dieser anaeroben Mikroorganismen wurde nach zwei Wissenschaftlern der Wood-Ljungdahl-Stoffwechselweg genannt.
Acetogene Bakterien sind nicht nur Supertalente der Biotechnologie, sondern auch Überlebenskünstler unserer Erde. Es wird angenommen, dass sie sich vor 4,5 Milliarden Jahren in Zeiten der Ur-Atmosphäre entwickelt haben. Heute reicht ihr natürliches Habitat, abhängig von der Art, von marinem Sediment über Flussschlamm bis Vogelkot. Der erste beschriebene Bakterienstamm, der aus H2 und CO2 autotroph und anaerob Acetat herstellen kann, ist Clostridium aceticum. Der Mikroorganismus kann neben CO2 auch CO als Kohlenstoffquelle nutzen.
Acetobacterium woodii und C. ljungdahlii sind die zwei Modellorganismen, mit denen der acetogene anaerobe Stoffwechsel näher erforscht wurde. Sie sind damit für die biobasierte CO2-Verwertung von großer Bedeutung.
Knallgasbakterien
Neben anaerob lebenden Mikroorganismen werden für die Gasfermentation auch aerobe Bakterienstämme genutzt. Die CO2-Fixierung erfolgt über den Calvin-Benson-Zyklus. Wasserstoff wird hierbei als Energiequelle genutzt, indem Sauerstoff zu Wasser reduziert wird. Der spektakuläre Name Knallgasbakterien leitet sich von der Reaktion zwischen Wasserstoff und Sauerstoff ab, bei der ein lauter Knall entsteht.
Das Knallgasbakterium Cupriavidus necator ist von Bedeutung in der Forschung, da es in der Lage ist, CO2 für die Herstellung von Polyhydroxyalkanoat (PHA) in einem Gasfermentationsverfahren zu verwenden. Die Bakterienkultur wird unter Fütterung mit einer organischen Kohlenstoffquelle vermehrt, zum Beispiel Bioabfälle. Darauf folgt die autotrophe Produktionsphase von PHA unter Begasung mit CO2 und H2. PHA ist als Bioplastik ein vielseitig einsetzbares Material in der Verpackungs- und Nahrungsmittelindustrie, aber auch für medizinische Applikationen. Für das Verfahren können auch CO2-haltige Abgas-Ströme der Industrie verwendet werden. Eine Herausforderung des Projekts ist die Hochskalierung auf den Industriemaßstab, da eine ausreichende Versorgung mit H2 und O2 Explosionsgefahr birgt und somit hohe sicherheitstechnische Anforderungen mit sich bringt.
In den vergangenen Jahren wurden viele weitere Vertreter der Knallgasbakterien isoliert und charakterisiert. Ihr Stoffwechsel und seine Regulation sind dennoch bislang nicht gut verstanden und die meisten Aktivitäten befinden sich noch im Bereich der Grundlagenforschung.
Forschungs- und Entwicklungsaktivitäten
Das BMBF unterstützt die Bestrebungen der biotechnologischen CO2-Verwertung mit zahlreichen Projekten. Seit 2022 gefördert wird das Projekt GasValor im Rahmen der Modellregion für Bioökonomie im Rheinischen Revier. Dessen Ziel ist die Verwertung von CO2 und Methan, die im Rheinischen Revier in Biogasanlagen, Kläranlagen und Industrieprozessen in große Mengen anfallen. Durch mikrobielle Gasfermentation sollen die Gase zu Acetat beziehungsweise PHA und Futtermitteladditiven umgesetzt werden.
Ein weiteres Projekt ist der Innovationsraum BioBall – Bioökonomie im Ballungsraum Frankfurt/RheinMain. Gefördert werden Technologien zur stofflichen Nutzung von in der Region vorhandenen biogenen Stoff- und Abfallströmen. Im Verbundvorhaben SynBioTech als Teil des Verbundprojekts wird biogenes CO2 zu Methanol hydriert, das anschließend durch Methylobacterium zu Biomasseprotein für die Futtermittelindustrie bzw. Säurederivaten für den chemischen Markt umgesetzt wird.
Video: Wenn aus Abgas Rohstoff wird
Die strategische Allianz ZeroCarbFP unter Federführung der Südzucker AG und der BRAIN Biotech AG hatte sich zum Ziel gesetzt, Enzyme und Mikroorganismen zu identifizieren, die für die Verwertung und Umwandlung von kohlenstoffreichen Abfallströmen zu Wertstoffen geeignet sind. Neben Forschungspartnern waren an diesem vom BMBF geförderten Verbundprojekt viele Industriepartner beteiligt wie Bioeton Deutschland, Fuchs Schmierstoffe, EMERY Oleochemicals und die Cronimet Mining AG.
Langkettige Kohlenstoffverbindungen mit hohem wirtschaftlichem Wert nachhaltig herzustellen, das ist das Ziel des BMBF-Forschungsprojekts Gas-Fermentation. Die Beteiligten der Universitäten Ulm, Stuttgart und München modifizieren gasverwertende Mikroorganismen so, dass sie Isobutanol, Isoprenoide, Hexanol und bifunktionelle Moleküle wie 1,4-Butandiol und 1,6-Hexandiol herstellen können.
Das Projekt ThermoSynCon dreht sich um die Entwicklung thermophiler Mikroorganismen als Biokatalysatoren für die heiße Synthesegas-Fermentation. Im Vergleich zu bisher für die Gasfermentation genutzten Bakterienstämmen können thermophile Organismen bei einer Temperatur von 50 bis 80 Grad Celsius optimal arbeiten. Die Projektbeteiligten charakterisieren bisher unbekannte hitzeliebende, acetogene Bakterienstämme. Im nächsten Schritt sollen genetische Werkzeuge verbessert werden, um thermophile Acetogene im Hinblick auf ihre Anwendung als industrielle Plattformorganismen zu verändern.
An der Universität Tübingen wird geforscht, wie bei der Gasfermentation Mikroorganismen in Mischkultur optimal zusammenarbeiten können. Das Projekt ist Teil von internationalen Entwicklungs- und Forschungsaktivitäten am Novo Nordisk Foundation CO2 Research Centers in Norwegen. Es ist ein Zusammenschluss der Industrie mit Forschenden aus Norwegen, den USA und Niederlanden, Dänemark und Deutschland. Der Fokus liegt auf Technologien zur Abscheidung, Speicherung und Wiederverwertung von CO2.
Auch die Fraunhofer-Gesellschaft betreibt institutsübergreifend anwendungsnahe Projekte rund um die Fragestellung, wie CO2 aus Industrieabgasen mithilfe mikrobieller Fermentationsverfahren verwertet werden kann. So setzt das Projekt EVOBIO bei Kläranlagen an, um dort Stoffkreisläufe zu schließen und neben Nährstoffen auch CO2 zurückzugewinnen und einer direkten stofflichen Nutzung zuzuführen. Das Forschungsprojekt ShaPID will CO2 und biogene Rohstoffe einsetzen, um daraus neue Polymere für die Kunststoffindustrie herzustellen.
Die Gasfermentation kann auch mit elektrochemischen Prozessen gekoppelt werden. In dem Projekt CELBICON kombinieren die Forschenden die Absorption von CO2 aus der Luft mit der elektrochemischen CO2-Umsetzung zu kohlenstoffbasierten Zwischenprodukten und einer abschließenden mikrobiellen Fermentation dieser Zwischenprodukte zu höherwertigen Chemikalien.
In dem Forschungsprojekt Rheticus wird das Prinzip der Gasfermentation mit der Elektrolyse gekoppelt. Evonik und Siemens arbeiten gemeinsam an dem biohybriden Power-to-X-System, bei dem CO2 mit erneuerbarer Energie und anschließend durch Fermentation in Chemikalien umgewandelt wird. CO2 aus industriellen Abgasen wird in CO und H2 umgewandelt, was später durch mikrobielle Gasfermentation zur Herstellung der Chemikalien Butanol und Hexanol verwendet wird. Diese können für Kunststoffe, Nahrungsergänzungsmittel und Treibstoffe genutzt werden. Das BMBF fördert die Forschungsprojekte Rheticus I und II mit insgesamt 6,3 Mio. Euro.
Video: Rheticus-Projekt – Wie aus CO2 grüne Chemie wird
Relevante Wirtschaftsakteure
Bei der Kommerzialisierung der Gasfermentationstechnologie ist das US-amerikanische Unternehmen LanzaTech führend. Die Firma gilt als Pionier der mikrobiellen Abgasverwertung und hat 2018 die erste industrielle Gasfermentationsanlage zur Ethanol-Herstellung in Caofeidian (China) in Betrieb genommen. LanzaTech nutzt das Bakterium Clostridium autoethanogenum zur Umsetzung von CO in Ethanol. Außerdem kann der Organismus das C4-Produkt 2,3-Butandiol herstellen. Kohlenstoffquelle sind Stahlwerksabgase.
In dem Prozess werden die energiereichen Abgas- und Restströme in einen Blasensäulenreaktor geleitet, in welchem sich die Mikroorganismen befinden. Die Produkte werden später von der Fermentationsbrühe abgetrennt und können weiterverarbeitet werden, zum Beispiel zu Nylon, Kunststoffen, Kautschuk und Treibstoff. Eine der Hürden der biologischen Gasfermentation konnte das Unternehmen durch technologischen Fortschritt überwinden, nämlich die geringe Löslichkeit der gasförmigen Substrate CO und H2. Die firmeneigene Technologie umfasst eine Mikroblasen-Erzeugung, um den Stoffaustausch an der Oberfläche entsprechend zu verbessern.
Laut Konzern werden 60 Millionen Liter Ethanol pro Jahr in China (Stand 2017) produziert. Neben dem Werk in China wurde 2020 auch ein Produktionswerk in Gent (Belgien) errichtet. Laut LanzaTech kann die firmeneigene Technologie die Treibhausgas-Emissionen der Ethanol-Produktion um 70 % senken, verglichen mit herkömmlichen, auf fossilen Rohstoffen basierenden Technologien.
Statt Ethanol werden bei Arkeon Biotechnologies, einem Start-up aus Wien, aus CO2 Proteine hergestellt, die in der Lebensmittelindustrie genutzt werden. Für die Umsetzung werden industrielle Kohlenstoff-Abscheidungen und Archaeen als Mikroorganismen genutzt, die anaerob in einer salzhaltigen Lösung wachsen können. Für den marktwirtschaftlichen Eintritt werden nach Angaben der Gründer noch etwa zwei Jahre benötigt.
Das Unternehmen Superbrewed Foods (ehemals White Dog Labs) hat eine neuartige anaerobe, mixotrophe Fermentation unter der Bezeichnung MixoFermTM entwickelt, bei der gleichzeitig Zucker und die Gase CO und H2 im selben acetogenen Bakterium verstoffwechselt werden. Mit dieser Technologie wird die Massenausbeute von Produkten und somit die Wirtschaftlichkeit der Prozesse gesteigert.
Das hessische Start-up CO2BioClean verfolgt das Ziel, CO2 als Rohstoff für die Herstellung natürlicher Biopolymere zu verwenden. Mit einem patentierten Fermentationsverfahren erzeugt das junge Unternehmen aus dem Treibhausgas vollständig biologisch abbaubare Textilfasern. Neben Polyhydroxyalkanoat (PHA) gehört Polyhydroxybuttersäure (PHB) zu den Produkten des vom European Innovation Council (EIC) geförderten Unternehmens.
Seite 4 von 7
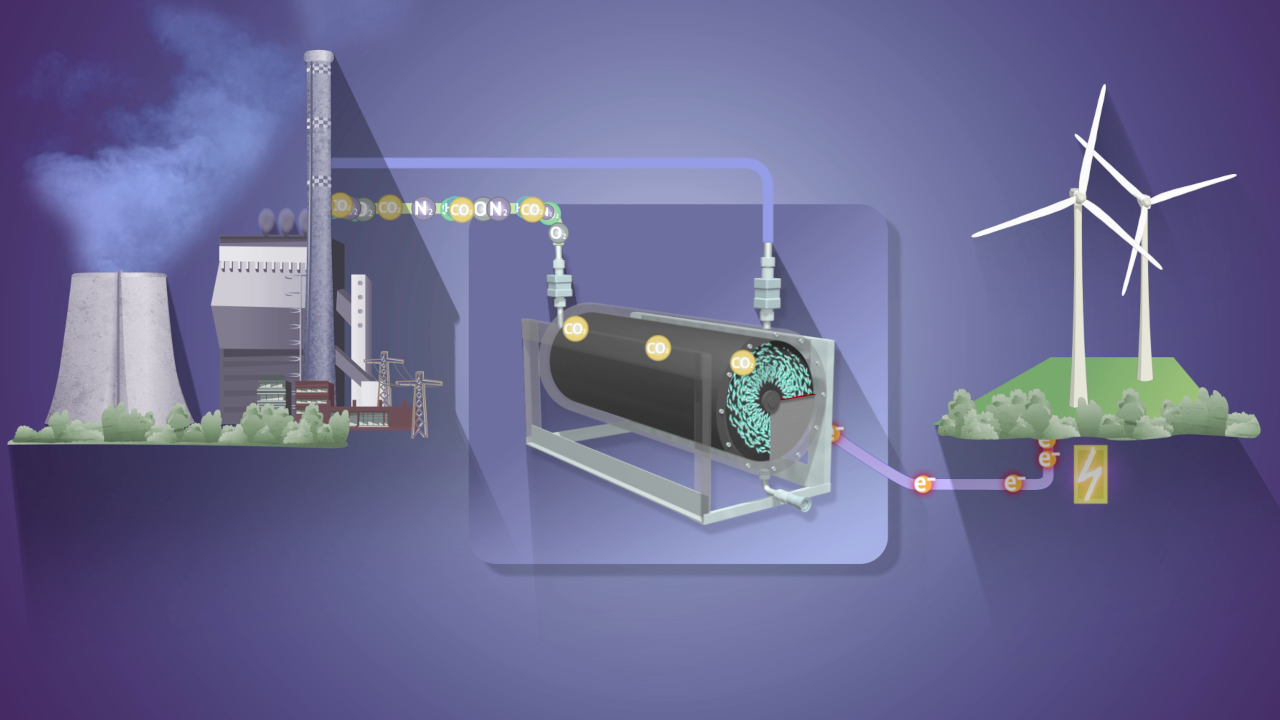
Elektrobiosynthesen: Strombasiert CO2 verwerten
Die Elektrobiosynthese, auch biobasierte Elektrokatalyse oder mikrobielle Elektrosynthese genannt, ermöglicht ein stromgetriebenes Nutzen von Biokatalysatoren zur Herstellung von verschiedenen chemischen Produkten. Energetisch unvorteilhafte Biosynthesen wie die Reduktion von CO2 können durch das Zuführen von elektrischer Energie angetrieben werden. Entsprechend ist die Elektrobiosynthese eine vielversprechende Technologie für die Wiederverwertung von CO2.
Im Labormaßstab konnte ein breites Spektrum an Produkten hergestellt werden, darunter sowohl Methan, Methanol oder Ethanol, aber auch höherwertige Produkte wie langkettige Alkohole (Isopropanol, Hexanol, Butanol), Terpene oder Biokunststoffe (PLA/PBA). Die Forschung befindet sich jedoch noch im Grundlagenbereich.
Für die Produktion werden Elektroden direkt in einen Bioreaktor integriert. Mikroorganismen besiedeln diese Elektroden als Biofilm und tauschen Elektronen aus. Die Organismen nutzen CO2 als Substrat und die elektrische Energie, um das Gas in ein Produkt umzuwandeln. Genau wie bei der Gasfermentation sind Acetogene sowie Knallgasbakterien geeignete Biokatalysatoren für die Elektrobiosynthese. Die benötigte elektrische Energie sollte aus erneuerbaren Quellen stammen, damit die CO2-Verwertung nachhaltig abläuft.
In dem Projekt METAFOR untersuchen Forschende der RWTH Aachen, wie Produkte der Elektrobiosynthese mithilfe von Hefen zu Basischemikalien aufgewertet werden können. Das CO2 wird elektrochemisch zu den C1-Verbindungen Methanol und Formiat (Salz der Ameisensäure) reduziert. Diese werden anschließend von der methylotrophen Hefe Ogataea polymorpha zu Wertprodukten aufgebaut.
Das BMBF fördert außerdem das Projekt MES 2.0 (Mikrobielle Elektrosynthese) des DECHEMA Forschungsinstituts. Auch hier ist die Kopplung der elektrochemischen Synthese mit mikrobieller Stoffproduktion von Bedeutung. Die Forschenden untersuchen das gezielte Anheften und die anschließende Biofilmbildung der elektroaktiven Mikroorganismen auf den Elektrodenmaterialien.
Ein fundamentales Verständnis von elektrochemisch aktiven mikrobiellen Biofilmen zu ermöglichen ist eines der Forschungsziele des Helmholtz-Zentrums für Umweltforschung in Leipzig. Außerdem sollen neue, ökonomisch relevante bioelektrotechnologische Syntheserouten und Reaktoren für die oxidative und reduktive Erzeugung von Plattform- und Feinchemikalien entwickelt werden.
Das Fraunhofer-Projekt eBioCO2n umfasst stromgetriebene CO2-Konversion durch synthetische Enzymkaskaden zur Herstellung von Spezialchemikalien. Im Fraunhofer-Max-Planck-Kooperationsprogramm geht es um die elektrobiokatalytische Verwertung von CO2 mit Enzymen.
Die mikrobielle Elektrosynthese befindet sich noch in einem frühen Entwicklungsstadium und ist bisher nur auf den Labormaßstab beschränkt. Doch das belgische Unternehmen VITO hat sich den Bau und Betrieb eines Pilotreaktors für die mikrobielle Elektrosynthese zum Ziel gesetzt. Das Vorhaben wird unterstützt durch ein vom Unternehmen geleitetes Forschungsprojekt, bei dem durch mikrobielle Elektrosynthese Proteine hergestellt werden sollen.
Für eine Maßstabsvergrößerung der mikrobiellen Elektrosynthese muss die Produktextraktion und -aufreinigung zur Gewinnung weiterer Substanzen verbessert werden. Das Flächenwachstum der Mikroorganismen auf den Elektroden stellt ebenfalls eine Limitierung für die Skalierung der Prozesse auf industrielle Maßstäbe dar. Forschungsbedarf besteht in der Aufklärung der grundlegenden biochemischen Prozesse, der Entwicklung neuer Bioreaktorkonzepte und der Skalierung und Entwicklung von Produktionsprozessen, die industriellen Anforderungen entsprechen.
Seite 5 von 7
Photosynthese-Prozesse nutzen: Photoautotrophe Mikroalgen und Bakterien
Mikroalgen und andere photosynthetisch aktive Mikroorganismen können auf ganz natürlichem Weg CO2 umsetzen. In der Biotechnologie werden sie genutzt, um hochwertige Chemikalien herzustellen. So werden Komponenten wie Antioxidantien, Pigmente und Proteine aus der Algenbiomasse extrahiert und als Nahrungsergänzungsmittel genutzt. Auch Biokraftstoffe können mit Mikroalgen hergestellt werden. Darüber hinaus stellen sie eine ideale Quelle für Biomasse dar, die sich als hochwertiges Futtermittel nutzen lässt. So kann CO2 optimal wiederverwertet werden, ganz nach dem Vorbild der Natur.
Algen als CO2-Speicher
Mithilfe von Algen wird in dem vom BMBF geförderten Projekt GreenCarbon an Herstellungsverfahren für Polymere und carbonfaserbasierte Leichtbaumaterialien geforscht. Diese können in der Automobilbranche und Flugzeugindustrie eingesetzt werden. In dem Herstellungsprozess werden die Mikroalgen als Nahrungsgrundlage für ölbildende Pilze eingesetzt. Das Öl kann anschließend in die Komponenten von Leichtbaumaterialien chemisch überführt werden.
Auch in der Landwirtschaft könnte die Algenkultivierung vielversprechende Geschäftsfelder eröffnen. Damit beschäftigte sich das vom Bundesministerium für Ernährung und Landwirtschaft geförderte Verbundprojekt FuTuReS. Im Fokus steht die Mikroalge Phaeodactylum tricornutum. Erste Ergebnisse zeigen die Profitabilität des Farbstoffs Fucoxanthin und der Omega-3-Fettsäure Eicosapentaensäure (EPA) als Produkte der Algenzucht.
Wie das schon heute funktionieren kann, zeigt Landwirt Maarten Heins. Er integriert die Algenzucht in seinen landwirtschaftlichen Betrieb und entwickelt sich somit ein zweites Standbein. In dem Video aus der Reihe der Biopioniere erzählt er unter anderem davon, wie stolz er auf die Zucht der Mikroalge Spirulina ist, welche er als Nahrungsergänzungsmittel weiterverkauft.
Video: Biopioniere-Porträt über Maarten Heins – Der Algenbauer
Die Mechanismen der biologischen CO2-Verwertung durch Photosynthese sind Gegenstand langjähriger Forschung. Zum einen wird versucht, die Photosynthese für die Produktion spezifischer Produkte einzusetzen. Zum anderen arbeiten Experten an Möglichkeiten, die Photosynthese zu optimieren und für andere Prozesse zu nutzen.
In dem Projekt Bio-Photovoltaik des Helmholtz-Zentrums für Umweltforschung wird die Kraft der Photosynthese mit einem elektrochemischen System erweitert. Cyanobakterien werden genutzt, um aus Wasser, CO2 und Sonnenlicht energiereichen Wasserstoff zu produzieren. Die bei der Photosynthese freiwerdenden Elektronen werden dabei auf ein elektrochemisches System übertragen, um reinen Wasserstoff zu erzeugen.
Im Rahmen des Forschungskonsortiums MaxSynBio, unterstützt durch das BMBF im Rahmen der Förderinitiative Biotechnologie 2020+, forschte unter anderem das Team von Tobias Erb am CETCH-Zyklus. Durch ihn soll CO2 aus der Atmosphäre während der Photosynthese effektiver umgesetzt werden. Verwendet wird das Kohlenstoff-bindende bakterielle Enzym Crotonyl-CoA Carboxylase/Reductase (CCR). Zusammen mit weiteren Enzymen lässt sich das Enzym CCR im Reagenzglas zum CETCH-Stoffwechselweg zusammenfügen. Der künstliche Zyklus wandelt Kohlendioxid effektiver um als der von Pflanzen genutzte Calvin-Zyklus und könnte eines Tages in Pflanzen und Algen eingesetzt werden, um überschüssiges CO2 aus der Atmosphäre zu binden und in nützliche organische Substanzen umzuwandeln.
Video: Photosynthese-Forscherin Kirstin Gutekunst im Porträt
Die grünen Bakterien in der Wirtschaft
PhotoBionicCell heißt das Projekt der Firma Festo in Zusammenarbeit mit dem Max-Planck-Institut für terrestrische Mikrobiologie in Marburg. Die Forschenden nutzen das Cyanobakterium Synechocystis, um auf Basis von CO2 Farbpigmente, Omega-3-Fettsäuren und Polyhydroxybuttersäure (PHB) herzustellen. PhotoBionicCell wird von einer Software komplettiert, welche es möglich macht, mehrere Photobioreaktoren live aus der Ferne zu überwachen, manuelle Parameteränderungen und Auswertungen vorzunehmen und die Produkternte ferngesteuert einzuleiten.
Das niederländische Unternehmen Photanol kommerzialisiert die Nutzung von Cyanobakterien zur Herstellung chemischer Rohstoffe. Die genetisch veränderten Organismen nutzen CO2 als Grundlage, um Rohstoffe wie L-Milchsäure herzustellen. L-Milchsäure wird zur Erzeugung des Biopolymers Polymilchsäure (PLA) eingesetzt.
Seite 6 von 7
Öffentliche Förderaktivitäten
Biotechnische Prozesse, die CO2 und andere C1-Moleküle als Rohstoff für die Chemikalienproduktion nutzen, schneller in die industrielle Anwendung bringen – das ist das Ziel der neuen Förderrichtlinie „CO2Biotech – Klimaneutrale Produkte durch Biotechnologie” des BMBF.
Mit der Ausschreibung im Rahmen der Nationalen Bioökonomiestrategie sollen die Potenziale der Biotechnologie für die CO2-Verwertung erschlossen werden, um Deutschlands Rolle als Entwickler und Anbieter moderner Technologien für klimaneutrale Produktionsprozesse zu stärken und die Abhängigkeit von Importen fossiler Rohstoffe zu senken. Gefördert werden Forschungs-, Entwicklungs- und Innovationsvorhaben, die biotechnologische Verfahren und Prozesse der CO2-Nutzung auf ihrem Weg in die industrielle Anwendung entscheidend voranbringen.
Forschungsansätze, die für eine Förderung infrage kommen, sind unter anderem:
- Biotechnische Verfahren zur CO2-Fixierung und -Umsetzung (wie die in diesem Dossier beschriebene Gasfermentation)
- Biohybride Verfahren oder Elektrobiosynthese zur CO2-Reduktion und Umsetzung
- C1-Fermentationen
Die Kombination biotechnologischer und nicht-biotechnischer Prozessschritte bietet die Aussicht auf besonders effiziente und nachhaltige Gesamtprozesse. Deshalb seien derartige integrierte Kombi-Verfahren von hohem Interesse, heißt es im Ausschreibungstext. Die Frist zur Einreichung von Projektskizzen war der 11. Januar 2023.
CO2Biotech: Klimaneutrale Produkte durch Biotechnologie
Details zur Fördermaßnahme gibt es auf der BMBF-Website: Klimaneutrale Produkte durch Biotechnologie – CO2BioTech.
FONA-Förderung
Die Initiative CO2-WIN ist Teil des Rahmenprogramms „Forschung für Nachhaltige Entwicklung – FONA3“. Die BMBF-Förderrichtlinie fokussiert auf die Bereiche elektrochemische Umwandlung von CO2, chemische und biotechnologische Prozesse zur Produktion nachhaltiger Chemikalien und Kraftstoffe sowie die Mineralisierung mittels CO2 zur Herstellung klimaschonender Baustoffe.
Auch mit dieser Fördermaßnahme will das BMBF die Nutzung von CO2 als nachhaltige Kohlenstoffquelle weiter vorantreiben, um die Rohstoffbasis der deutschen Wirtschaft zu verbreitern und gegen Versorgungskrisen abzusichern.
Kopernikus-Projekte
Thematische Schwerpunkte der Förderung sind die direkte Nutzung von Sonnenlicht zur Umwandlung von CO2, innovative Verfahren zur Reduktion von CO2 mit Anwendungsbezug und die Entwicklung biotechnologischer oder chemisch-biotechnologischer Verfahren zur stofflichen Nutzung von CO2.
Das Projekt Power-to-X (P2X) erforscht die Umwandlung von erneuerbar erzeugtem Strom in Gase, Kraftstoffe, Chemikalien und Kunststoffe. Das Projekt gehört zu den Kopernikus-Projekten, eine der größten Forschungsinitiativen der Bundesregierung zum Thema Energiewende.
Die biotechnologische Verwertung von CO2 ist Teil des Projekts Power-to-Fuel (Strom zu Sprit). Dabei wird aus der Luft oder aus Abgasen gewonnenes CO2 verwendet, um klimafreundlichen Kraftstoff herzustellen. Eine weitere Forschungsfrage der P2X-Projekte ist, wie mithilfe von Mikroorganismen CO2 in großem Maßstab in Chemikalien umgewandelt werden kann, die der Kosmetikbranche Grundstoffe für Pflegeprodukte liefern.
Seite 7 von 7
Weitere Informationen und Quellen
Mehr auf bioökonomie.de
Hauptquellen für die Recherche
Kircher, M. & Schwarz, T. Hrsg. (2020). CO2 und CO – Nachhaltige Kohlenstoffquellen für die Kreislaufwirtschaft. Springer Berlin Heidelberg
Institut für Bioverfahrenstechnik (2021). Machbarkeitsstudie im Themenfeld Carbon Economy: Modulare Abgas-Raffinerie mit biologischen und hybriden Technologien mit Schwerpunkt auf CO2 -Recycling aus CO2 -Punktquellen
Fraunhofer-Institut für System- und Innovationsforschung ISI. (2020). Technologie- und Marktstudie: Übersicht über Technologien zur bioinspirierten CO2-Fixierung und -Nutzung sowie der Akteure in Baden-Württemberg