Nicht weniger als ein vollständig neues Verfahren zur Genom-Editierung – das hatte sich das Forschungsprojekt getLight (Novel light-inducible genome editing technology for crops) zum Ziel gesetzt. Damit wäre beispielsweise in der Pflanzenzüchtung die schnelle und präzise Entwicklung verbesserter Sorten möglich, ohne dass teure Lizenzgebühren für etablierte Verfahren wie CRISPR-Cas anfielen. Für den Machbarkeitsnachweis hat die Projektdauer von Juni 2018 bis Mai 2020 zwar nicht gereicht, doch wichtige erste Schritte konnten die Forschenden vom Fraunhofer-Institut für Molekularbiologie und Angewandte Oekologie IME auf dem Weg zu ihrem ehrgeizigen Ziel zurücklegen.
Lizenzkosten für CRISPR-Cas umgehen
„Für die Forschung ist CRISPR-Cas toll, weil man damit schnell Ergebnisse erzielen und publizieren kann“, erläutert Projektleiter Stefan Schillberg. „Am Fraunhofer-Institut sind wir aber an der Anwendung interessiert, und weil bei CRISPR andere die Patente haben, müssten unsere Industriepartner immer dafür bezahlen.“ Dadurch seien die Kosten in der Pflanzenzüchtung schnell so hoch, dass sie keiner mehr tragen wolle. „Mein Traum war es, stattdessen ein eigenes Verfahren hinzubekommen“, verrät der Biotechnologe. Den Ansatz dazu sollten sogenannte Quantum Cluster bilden. Die nötige Finanzierung über rund 500.000 Euro kam vom Bundesministerium für Bildung und Forschung (BMBF).
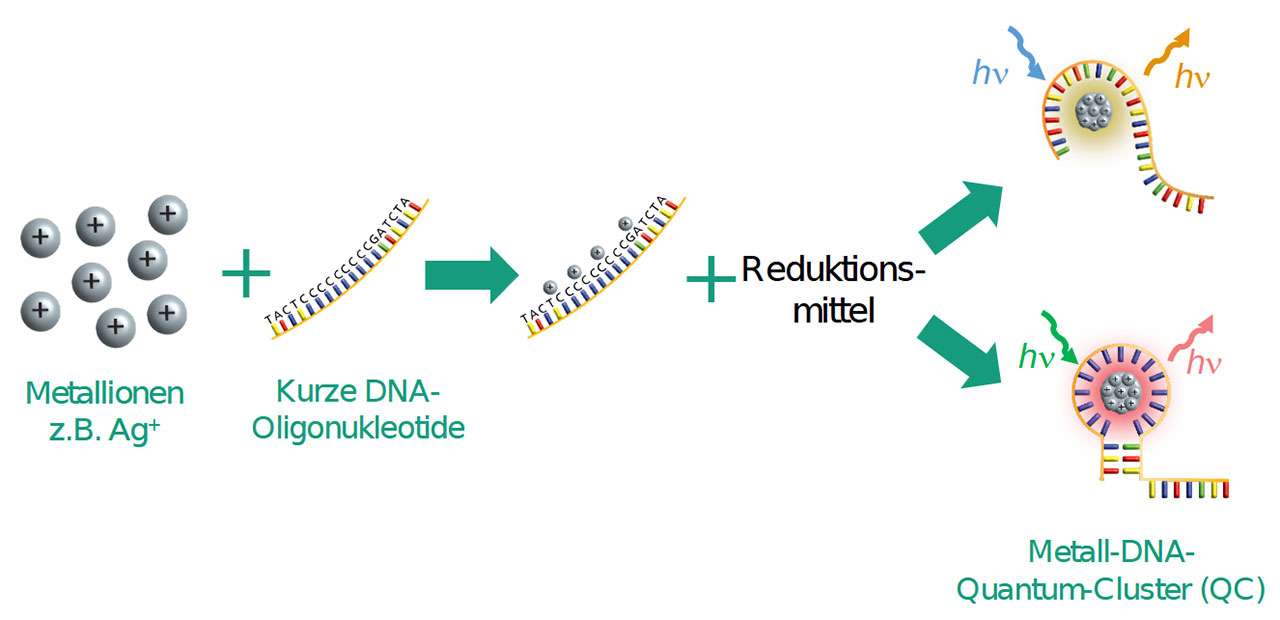
Als Quantum Cluster bezeichnen die Forschenden eine Verbindung aus einem kurzen DNA-Strang, der in der Zelle an die Zielsequenz koppeln kann, mit einer weiteren DNA-Struktur, beispielsweise einem sogenannten Loop, die Metallionen wie geladene Silberteilchen binden kann. Wird ein solcher Quantum Cluster mit Licht angeregt, fluoresziert er – je nach Wellenlänge, die auf ihn fällt, mit einer anderen Wellenlänge. Bislang werden solche Konstrukte in Nachweisverfahren genutzt, wo die Fluoreszenz entsprechend Aufschluss über den Aufenthaltsort des Quantum Clusters gibt.
Quanteneffekt erzeugt in der Theorie DNA-Brüche
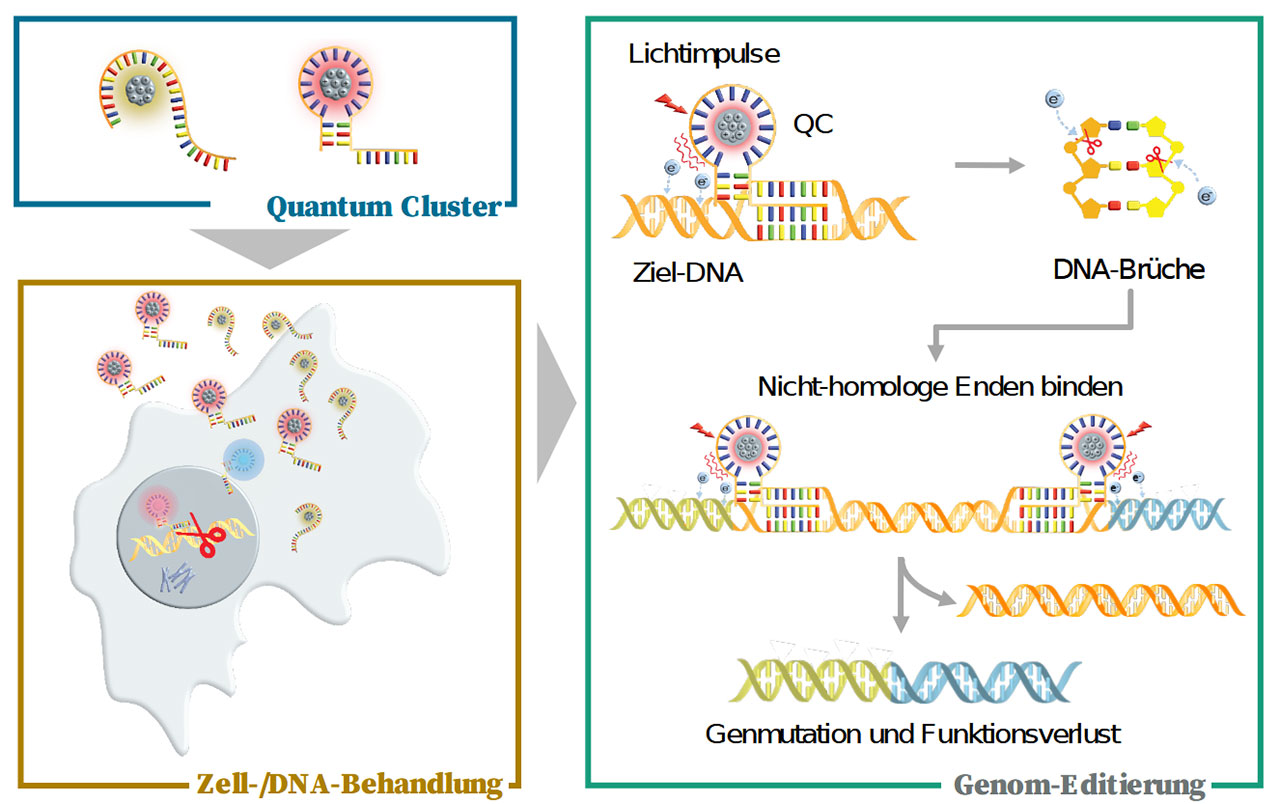
„Wir wollten diesen Effekt jedoch nutzen, um in der DNA Strangbrüche zu erzeugen“, erklärt Schillberg. Aus der Theorie ist bekannt, dass die durch die Fluoreszenz ausgestrahlten Photonen durch einen quantenphysikalischen Effekt, den sogenannten Tunneleffekt, Elektronen in Bewegung versetzen und dadurch in DNA-Strängen Brüche hervorrufen können. Auf diese Weise könnten kürzere oder längere DNA-Abschnitte ausgeschnitten und das betroffene Gen inaktiviert werden. „Die Idee ist, dass mit dieser Methode sehr präzise Eingriffe möglich wären, wenn man die richtige Sequenz auswählt, weil der Energietransfer nur während der Anregung stattfindet“, stellt der Forscher einen wichtigen Vorteil heraus. Auch CRISPR-Cas zeichnet sich durch eine hohe Präzision aus. Aber weil die molekularen Werkzeuge sich dabei dauerhaft in der Zelle befinden, geht Schillberg davon aus, dass ein zeitlich begrenzter lichtinduzierter Prozess wie bei getLight weniger Off-target-Effekte hätte, also seltener die DNA an Stellen verändern würde, wo das nicht gewünscht ist.
„Im Projekt haben wir erreicht, dass wir auf recht einfache Art Quantum Cluster herstellen können, die zudem relativ stabil sind“, berichtet Schillberg. Ersteres wäre ein Vorteil, um mit anderen Methoden der Genom-Editierung zu konkurrieren. Letzteres ist wichtig, wenn diese Nanopolymere später nicht nur im Reagenzglas, sondern in der Zelle ihre Funktion erfüllen sollen. „Diese Quantum Cluster lassen sich mit Licht anregen und binden in vitro auch an ihre Zielsequenz.“ Außerdem gebe es erste Hinweise, dass dort auch Strangbrüche stattfinden. „Aber wir haben dafür noch keinen eindeutigen Nachweis, dass das genau so funktioniert, wie wir es uns vorstellen“, relativiert der Projektleiter. Dafür sei die Entwicklung zu grundlegend und die Projektlaufzeit zu kurz gewesen. Seit Projektende arbeitet das Forschungsteam nebenher an seinem Ansatz weiter und ist auf der Suche nach einer Anschlussfinanzierung. „Es wäre schade, wenn wir das nicht fortführen können“, findet Schillberg.
Offene Fragen nach Projektende
Während die Herstellung der Quantum Cluster sich damit als unerwartet einfach erwiesen habe, sei alles Übrige komplexer als vermutet, resümiert der Biotechnologie. Wolle man die Methode weiterentwickeln, gehe es vor allem darum, weitere Quantum Cluster herzustellen und zu erproben, und dafür auch die richtigen Bedingungen zunächst in vitro und später in vivo herzustellen, damit der Strangbruch wie gewünscht funktioniert. „Ob wir beispielsweise eine feinere Einstellung der Lichtbestrahlung für die Elektronenanregung oder Kombinationen aus mehreren Quantum Clustern und Lichtquellen verwenden müssen – das konnten wir im Laufe des Projekts alles noch nicht vollständig entschlüsseln“, sagt Schillberg. Er hoffe, dass sich die Mittel finden werden, auch diese Fragen zu klären – denn die Einschätzung, dass der Ansatz von getLight nicht funktionieren könne, die habe er aus der Forschungscommunity nicht gehört.
Autor: Björn Lohmann


