Einleitung
Die Synthetische Biologie steht heute sinnbildlich für den nächsten Technologiesprung in den Lebenswissenschaften. Sie kombiniert das Design-Denken der Ingenieurwissenschaften mit den Möglichkeiten der Molekularbiologie und verändert damit grundlegend, wie wir biologische Systeme verstehen, nutzen und gestalten. Was früher noch Science-Fiction war, ist inzwischen wissenschaftliche Realität: Zellen können programmiert, Proteine computergestützt entworfen und Stoffwechselwege völlig neu konstruiert werden mit dem Ziel, CO₂ zu fixieren, nachhaltige Materialien zu erzeugen oder maßgeschneiderte Wirkstoffe zu entwickeln. Diese Disziplin ermöglicht nicht nur neue Produkte, sondern stellt gängige Produktionsparadigmen in Frage – von der chemischen Industrie bis zur Landwirtschaft. Die Synthetische Biologie ist dabei nicht nur eine Ergänzung klassischer Biotechnologie, sondern eine technologische Revolution an der Schnittstelle von IT, Genetik und Ingenieurwesen.

Im Zuge der Hightech Agenda Deutschland der Bundesregierung wird die Nationale Bioökonomiestrategie seit 2025 mit einem Fokus auf Zukunftstechnologien ergänzt. Das erklärte Ziel: Eine messbare Steigerung der internationalen Wettbewerbsfähigkeit, Nachhaltigkeit und technologischer Souveränität, auch mithilfe der Biotechnologie als eine von sechs Schlüsseldisziplinen. Ein wichtiger Schritt für die biobasierte Transformation ist die Verknüpfung von ingenieurwissenschaftlichen Prinzipien mit dem genetischen Potenzial biologischer Systeme. Genau dort setzt die Synthetische Biologie an.
Seite 2 von 6
Synthetische Biologie damals und heute
Schon heute hat das Forschungsfeld der Synthetischen Biologie eine beeindruckende Entwicklung hinter sich: Von seinen Ursprüngen in der De-Novo-Entwicklung lebensfähiger Minimalzellen über die modulare Nutzung zellulärer Komponenten reicht die Anwendung von hochentwickelten, biotechnologischen Verschaltungen von Stoffwechselwegen (engl. sophisticated metabolic engineering) heute in eine Vielzahl von potenziellen Anwendungen hinein.
Die Synthese von DNA-Molekülen, die vormals der Inbegriff der Synthetischen Biologie war, ist heute für alle Akteure schnell und kostengünstig verfügbar und stellt die Grundlage für die biotechnologische Produktentwicklung dar. Hinzu kommen durch den Fortschritt der Informationstechnologie Verknüpfungen mit computergesteuerter Simulation und künstlicher Intelligenz, die etwa Strukturvorhersagen von Proteinen ermöglichen. Ein prominentes Beispiel ist das Programm AlphaFold, das komplexe Proteinstrukturen basierend auf der zugrundeliegenden, linearen Aminosäuresequenz präzise berechnet.
Neben hochspezifischen Antikörpern und Wirkstoffen für die personalisierte Medizin sind vor allem neuartige Proteine, Produktionswege und Materialien für die Bioökonomie Gegenstand aktueller Forschungen. Die Möglichkeit, etwas völlig Neues zu schaffen, das über natürliche Vorbilder hinausgeht (engl. new-to-nature), hebt die Synthetische Biologie von der klassischen Stoffwechselmodifikation durch gentechnische Verfahren ab. Sie ist ein disruptives, multidisziplinäres Forschungsfeld und zahlt damit auf wichtige Ziele der Hightech Agenda Deutschland ein.
Seite 3 von 6
Natur neu denken: biologische Baupläne für modernes Wirtschaften
Die Basis der Synthetischen Biologie und ihrer Nutzung für die industrielle Bioökonomie liegt nicht in der bloßen Optimierung, sondern im Design und Neudesign biologischer Systeme und damit in der Schaffung von Funktionen, die in der Natur so nicht vorkommen. Am Max-Planck-Institut für terrestrische Mikrobiologie in Marburg arbeitet die Forschungsgruppe um Prof. Dr. Tobias Erb an der Neukonstruktion eines zentralen biochemischen Prozesses: der Photosynthese.

In der Natur setzt dieser bekannte Stoffwechselvorgang die Energie der Sonne nur zu etwa 5 % um und nutzt sie größtenteils zum Aufbau von Biomasse. Die geringe Effizienz beruht auf der unvollständigen Lichtnutzung, Wärmeabgaben und dem begrenzten Wirkungsgrad des Photosyntheseapparats selbst. Durch die Methoden der Synthetischen Biologie gelang es Erb und seinem Team, einen vollkommen neuartigen, in der Natur nicht vorkommenden Stoffwechselweg zu entwerfen, den sogenannten CETCH-Zyklus. Dieser synthetische CO₂-Fixierungsweg kombiniert Enzyme aus verschiedenen Organismen und funktioniert sowohl in zellfreien Systemen als auch in lebenden Zellen und Bioreaktoren. Er benötigt nur 24 bis 28 Lichtquanten pro gebundenem CO₂-Molekül, während die natürliche Photosynthese etwa 34 benötigt. Das entspricht einer Effizienzsteigerung von rund zwanzig Prozent. Damit demonstriert der CETCH-Zyklus eindrucksvoll, welchen Beitrag das rationale Design biologischer Systeme zum Verständnis und zur technischen Nutzung biochemischer Prozesse leisten kann.
Während die klassische industrielle Biotechnologie meist darauf abzielt, bestehende Stoffwechselwege zu optimieren oder umzuleiten, eröffnet die Synthetische Biologie die Möglichkeit, völlig neue Stoffwechselarchitekturen und Produktpfade zu entwerfen bis hin zu künstlich designten Zellen. Dadurch lassen sich Produkte entwickeln, die in der Natur nicht vorkommen, oder natürliche Moleküle gezielt verändern, um neue Eigenschaften und Anwendungen zu erschließen, etwa maßgeschneiderte Biopolymere, Spezialchemikalien oder neuartige Wirkstoffe.
Weiteres Anwendungspotenzial der Synthetischen Biologie liegt in der Nutzbarmachung alternativer Rohstoffquellen. Durch gezieltes Design biologischer Systeme können Mikroorganismen so angepasst werden, dass sie industrielle Restströme oder Klimagase wie CO2 als Ausgangsstoffe nutzen. Damit trägt die Synthetische Biologie nicht nur zur Entwicklung neuartiger Produkte bei, sondern zugleich zur Transformation der industriellen Produktion hin zu einer kreislauforientierten und ressourcenschonenden Bioökonomie.
Seite 4 von 6
Aktuelle Forschung im Portrait
Das Bundesministerium für Forschung, Technologie und Raumfahrt (BMFTR) fördert im Rahmen verschiedener Richtlinien gezielt den Transfer biotechnologischer Innovationen in die Industrie. Besonders im Fokus: Projekte, die nicht nur technische Machbarkeit demonstrieren, sondern auch einen echten Nachhaltigkeitsbeitrag leisten. Die Synthetische Biologie ermöglicht dabei völlig neue Wege, um biologische Prozesse gezielt zu gestalten – schneller, effizienter und unabhängiger von endlichen Ressourcen.
CO₂ als Rohstoff: Wertschöpfung neu gedacht
Im Rahmen der Maßnahme „Klimaneutrale Produkte durch Biotechnologie – CO₂ und C1-Verbindungen als nachhaltige Rohstoffe für die industrielle Bioökonomie (CO2BioTech)“ wird das Projekt ValenCell an der Heinrich-Heine-Universität Düsseldorf gefördert. Dort wird mithilfe Synthetischer Biologie die Produktion des Aromastoffs Valencen in photoautotrophen Mikroalgen optimiert. Der große Vorteil an diesem Ansatz ist, dass anstatt Valencen energie- und ressourcenintensiv aus Zitrusfrüchten zu extrahieren, der Stoff nun gezielt im Photobioreaktor hergestellt werden kann und das klimafreundlich, unabhängig von landwirtschaftlicher Fläche und saisonalen Erträgen. Dieses Projekt zeigt beispielhaft, wie Synthetische Biologie die Rohstoffbasis ganzer Branchen transformieren kann.
Palmöl neu denken: Mikroben statt Monokulturen
Das Hamburger Start-up COLIPI setzt auf Gasfermentation, um nachhaltige Alternativen zu Palmöl herzustellen. Mikroorganismen wie Hefen und wasserstoff-oxidierende Bakterien werden mit CO₂-haltigen Abgasen und industriellen Nebenprodukten „gefüttert" und produzieren daraus hochwertige Öle. Mithilfe Synthetischer Biologie werden diese Mikroben gezielt auf Effizienz und Produktvielfalt hin optimiert. Die Vision: eine dezentrale, skalierbare und ressourcenschonende Ölproduktion kombiniert mit deutscher Bioverfahrenstechnik, die die herkömmliche Palmölindustrie langfristig ablösen. COLIPI wird sowohl im Rahmen der Fördermaßnahme „KMU-innovativ: Bioökonomie“ als auch in der Initiative „Bioökonomie international“ durch das BMFTR gefördert.

Kreislaufwirtschaft durch Synthetische Biologie
Im Programm „Circular Biomanufacturing“ der Bundesagentur für Sprunginnovation (SPRIN-D) zeigen drei Projekte eindrucksvoll, wie Synthetische Biologie Kreisläufe schließen kann:
- AmphiStar nutzt genetisch optimierte Hefezellen, um biogene Abfallstoffe in nachhaltige Biotenside zu verwandeln – eine umweltfreundliche Alternative zu herkömmlichen Tensiden aus fossilen Quellen. Der biotechnologische Prozess ermöglicht die flexible Nutzung regionaler Reststoffe und reduziert gleichzeitig CO₂-Emissionen.
- MATERI-8 entwickelt ein neuartiges Recyclingverfahren für komplexe Materialmischungen, die bislang nur durch Verbrennung entsorgt werden konnten. Hier kommen gezielt designte Mikroorganismen zum Einsatz, um Materialien selektiv abzubauen – ein paradigmatischer Wandel in der Abfallverwertung, möglich gemacht durch Synthetische Biologie.
- Das Unternehmen C3Biotech setzt auf ein salzliebendes Bakterium, das in der Lage ist, Grundstoffe für Acrylglas aus landwirtschaftlichen Reststoffen zu synthetisieren. Damit wird ein erdölbasierter Kunststoff durch ein biobasiertes, potenziell vollständig recycelbares Material ersetzt – ein zukunftsweisender Ansatz für eine nachhaltigere Kunststoffindustrie.
Klimaresiliente Landwirtschaft: beschleunigte Pflanzenzüchtung
Auch im Pflanzenbau eröffnet die Synthetische Biologie neue Möglichkeiten, insbesondere durch moderne Genom-Editierung und präzise Züchtungstechniken. Die BMFTR-Förderrichtlinie „Moderne Züchtungsforschung für klima- und standortangepasste Nutzpflanzen von morgen“ unterstützt 19 Forschungsprojekte, die auf resiliente Sortenentwicklung zielen.
Im Verbundprojekt POMORROW arbeiten fünf Forschungseinrichtungen und drei Züchtungsunternehmen mit Hilfe genetischer Ressourcen und innovativer Züchtungstechnologien an der Verbesserung der Kartoffel. Der gezielte Einsatz Synthetischer Biologie soll die Entwicklung robuster Sorten erheblich beschleunigen und an den Klimawandel angepasste Pflanzen schneller in die Praxis bringen.
Ein weiteres Schlüsselprojekt ist PROGRESS am IPK Gatersleben, das sich der Weiterentwicklung präziser Genom-Editierungswerkzeuge widmet. Ziel ist die Schaffung maßgeschneiderter Moleküle, die Verfahren wie CRISPR/Cas noch zielgerichteter und zugänglicher machen – eine essenzielle Grundlage für die Pflanzenzüchtung der Zukunft.
Synthetische Biologie trifft KI: Biodesign der nächsten Generation
Ein zentraler Treiber der aktuellen Entwicklung in der Synthetischen Biologie ist die zunehmende Automatisierung biologischer Prozesse durch sogenannte Biofoundries. Diese hochvernetzten, robotergestützten Labore ermöglichen die schnelle und präzise Umsetzung des sogenannten DBTL-Zyklus (Design–Build–Test–Learn). Von der Planung genetischer Konstrukte bis hin zur Validierung in lebenden Zellen laufen alle Schritte digital unterstützt, automatisiert und parallelisiert ab. Die Vorteile liegen auf der Hand: deutlich verkürzte Entwicklungszeiten, hohe Reproduzierbarkeit und die Möglichkeit, Tausende Varianten gleichzeitig zu testen. Besonders in Kombination mit künstlicher Intelligenz (KI) bieten Biofoundries eine bisher unerreichte Effizienz bei der Suche nach biologischen Lösungen für industrielle, medizinische und ökologische Herausforderungen. In Deutschland entstehen derzeit mehrere solcher Einrichtungen – teils an Universitäten, teils im Rahmen öffentlich geförderter Innovationszentren. Sie könnten künftig die Rolle eines „biotechnologischen Fertigungswerks“ übernehmen und den Transfer von Forschungsergebnissen in marktfähige Anwendungen radikal beschleunigen.
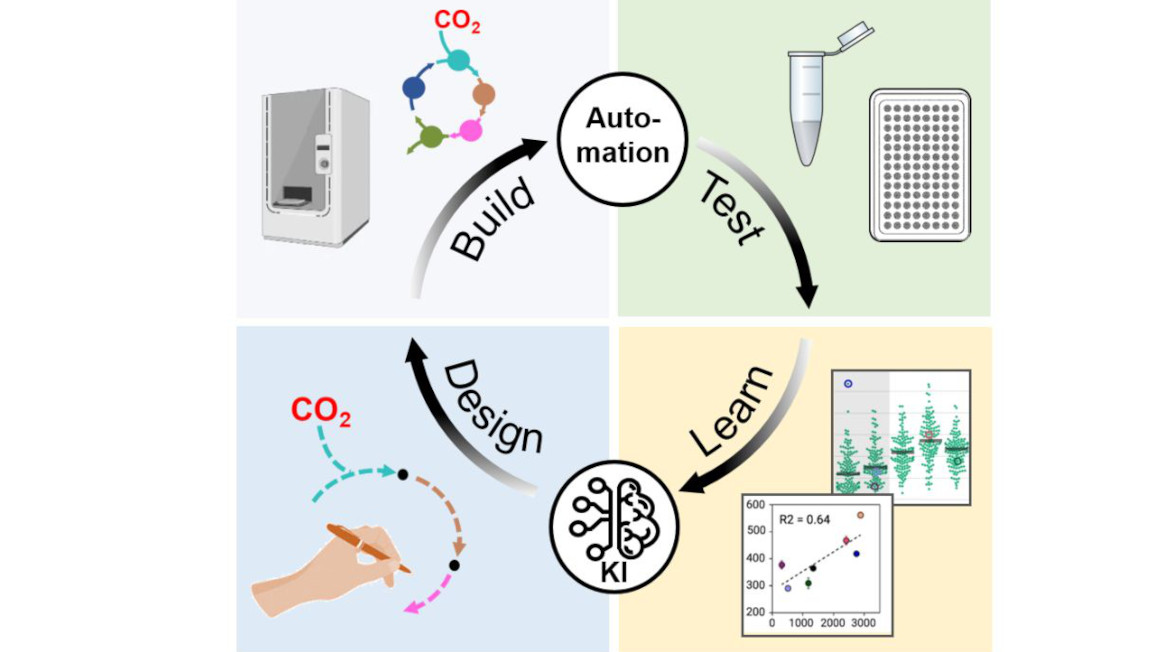
Einer der vielversprechendsten Trends ist dabei die Verknüpfung von Synthetischer Biologie mit KI-gestützten Designprozessen. Biotechnologische Innovation basierte bislang häufig auf langwierigen Trial-and-Error-Prozessen, ein Flaschenhals, den moderne Lernmodelle zunehmend durchbrechen. Cradle, ein niederländisch-schweizerisches Biotech-Unternehmen, nutzt etwa selbstlernende Algorithmen, um die Funktion von Enzymen und Proteinen digital zu entwerfen und zu optimieren. Das Berliner Start-up Cambrium geht noch einen Schritt weiter: Mit einem generativen Lernmodell werden neue biobasierte Materialien digital entwickelt, basierend auf gewünschten Eigenschaften wie Elastizität oder Hitzebeständigkeit. Erst danach erfolgt die Herstellung im Labor durch spezialisierte Mikroorganismen. Das erste Produkt, NovaColl™, ein veganes, hautidentisches Kollagen, zeigt exemplarisch das Potenzial dieses Ansatzes und brachte dem Team von Cambrium den Deep Tech Award 2024 ein.
Die Erweiterung der Synthetischen Biologie durch KI-gestützte Protein-Design-Technologien eröffnet zudem neue Perspektiven für die Kreislaufwirtschaft. Lernmodelle könnten künftig Neben- und Restströme aus der landwirtschaftlichen Produktion gezielt mit einbeziehen und so helfen, Treibhausgasemissionen weiter zu reduzieren. Die Programmierbarkeit biologischer Systeme erlaubt es Forschenden, mit wenigen Klicks neue Lösungsansätze für drängende ökologische und ökonomische Fragen zu entwerfen. Gleichzeitig bleibt entscheidend, dass technologische Dynamik und verantwortungsvolle Regulierung Hand in Hand gehen, damit Fortschritt in der Synthetischen Biologie nachhaltig und sicher gestaltet werden kann.
Mehr zum Thema KI in der Bioökonomie in der neuen Multimedia-Story.
Seite 5 von 6
Ausblick: die wichtige Rolle der Synthetischen Biologie für eine nachhaltige Bioökonomie
Neu designte Proteine, Materialien und Produkte eröffnen eine breite Palette von Anwendungen – von maßgeschneiderten Wirkstoffen über biobasierte Werkstoffe bis hin zu effizienten Bioraffinerien. Die Synthetische Biologie gilt als interdisziplinäre Ingenieurdisziplin, die biologische Systeme neu entwirft, baut und testet, mit Strukturen und Funktionen, die in der Natur so nicht vorkommen. So trägt sie nicht nur dazu bei, jene Ziele der Hightech Agenda Deutschland der Bundesregierung zu unterstützen, die auf resiliente Agrar- und Ernährungssysteme abzielen, sondern sie eröffnet darüber hinaus neue Wege in den Bereichen Gesundheit, Umwelt und nachhaltige industrielle Produktion.
Für die Bioökonomie eröffnet die Synthetische Biologie weit über bestehende biotechnologische Ansätze hinausgehende Perspektiven. Ihr besonderes Potenzial liegt nicht in der Optimierung bekannter Prozesse, sondern im Neudesign biologischer Systeme, Moleküle und Produktionswege und damit in der Fähigkeit, völlig neue Funktionen in oder außerhalb von lebenden Zellen zu schaffen. Unternehmen in Deutschland zeigen bereits, wie sich diese Technologie in marktfähige Innovationen übersetzen lässt: von CO₂-fixierenden Mikroorganismen über maßgeschneiderte Enzyme bis hin zu neuartigen, biobasierten Materialien. Mit einer gezielten Förderung, einer innovationsfreundlichen Regulierung und offenen Forschungsinfrastrukturen kann die Synthetische Biologie zu einem zentralen Motor einer nachhaltigen, wettbewerbsfähigen und klimaresilienten Bioökonomie werden.
Seite 6 von 6
Weiterführende Informationen
- Neue Technologien entwickeln: Hightech Agenda Deutschland (BMFTR, 2025): https://www.bmftr.bund.de/DE/Forschung/HightechAgenda/HightechAgenda_no…
- Was ist Synthetische Biologie? (Deutsche Gesellschaft für Synthetische Biologie (GASB)): https://gasb.de/de/what-is-synbio/
- Wie sich die Synthetische Biologie in Deutschland entwickelt (bioökonomie.de, 2022): https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/wie-sich…;
- Im Portrait | Cambrium: Neue Materialien mithilfe von KI (HealthCapital Berlin Brandenburg, 2024): https://www.healthcapital.de/news/artikel/cambrium-neue-materialien-mit…
- New European Biotech Act – Which way forward? (European Parliament Briefing, 2025): https://www.europarl.europa.eu/RegData/etudes/BRIE/2025/772866/EPRS_BRI…
- Förderrichtlinie: Klimaneutrale Produkte durch Biotechnologie – CO2 und C1-Verbindungen als nachhaltige Rohstoffe für die industrielle Bioökonomie (CO2BioTech) (BMFTR, 2022): https://www.bmftr.bund.de/SharedDocs/Bekanntmachungen/DE/2022/08/2022-08-19-Bekanntmachung-CO2BioTech.html
- Förderrichtlinie: Moderne Züchtungsforschung für klima- und standortangepasste Nutzpflanzen von morgen (BMFTR, 2023): https://www.bmftr.bund.de/SharedDocs/Bekanntmachungen/DE/2023/10/2023-1…;



