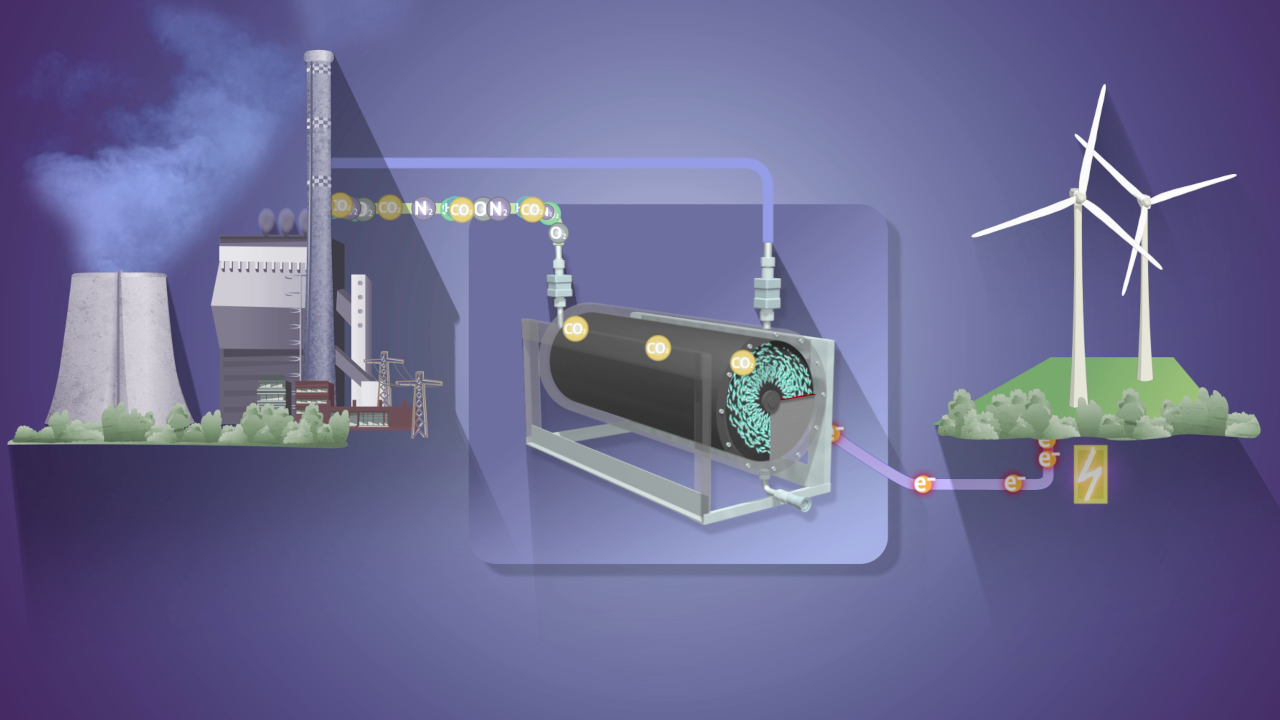
Polymermatrix ermöglicht neue Bioprozesse
Ein cleverer Ansatz erlaubt es, sauerstoffempfindliche Enzyme einzusetzen, um Biobrennstoffzellen zu betreiben und bald vielleicht auch Ammoniak herzustellen.

Enzyme sind in lebenden Zellen das, was Katalysatoren in der synthetischen Chemie sind: Sie machen die jeweilige Reaktion thermodynamisch erst möglich oder beschleunigen sie auf eine relevante Geschwindigkeit. Im Gegensatz zur klassischen Chemie benötigen Enzyme jedoch so gut wie nie teure Edelmetalle zur Katalyse, sondern besitzen in ihrem reaktiven Zentrum gut verfügbare Nichtedelmetalle. Das macht Enzyme für viele industrielle Anwendungen interessant. Einen Haken hat die Sache jedoch: Viele Enzyme reagieren empfindlich auf Sauerstoff.
Hochempfindliche Katalysatoren
„Solche hochempfindlichen Katalysatoren für Biobrennstoffzellen zu nutzen, ist nach wie vor eine der größten Herausforderungen bei der nachhaltigen Energieumwandlung“, sagt Wolfgang Schuhmann, Leiter des Zentrums für Elektrochemie an der Ruhr-Universität Bochum und Mitglied im Exzellenzcluster „Ruhr Explores Solvation“, kurz: Resolv. Gemeinsam mit zwei weiteren Forschungseinrichtungen haben die Bochumer ein Verfahren entwickelt, um zwei wichtige Enzyme trotz der eigentlich widrigen Reaktionsbedingungen höchst effektiv einzusetzen.
Hydrogenase für Biobrennstoffzelle
Im Fachjournal „Angewandte Chemie“ berichtet das Team um Schuhmann zusammen mit Kollegen vom Max-Planck-Institut für Chemische Energiekonversion in Mülheim an der Ruhr von einer Biobrennstoffzelle, in der die Forscher das Enzym Hydrogenase aus dem Bakterium Desulfovibrio desulfuricans nutzen konnten. Die Lösung bestand in einem sogenannten Redoxpolymer, in das das Enzym eingebettet wurde. Die Matrix aus dem Polymer verhindert den schädlichen Kontakt mit Sauerstoffmolekülen, ermöglicht aber den elektrischen Kontakt zwischen Enzym und Elektrode. Auf diese Weise gelang es, für Biobrennstoffzellen eindrucksvolle Leistungsdaten zu erzielen: Stromdichten von 14 Milliampere pro Quadratzentimeter und Leistungsdichten von 5,4 Milliwatt pro Quadratzentimeter.
Nitrogenase für Bioelektrosynthese
Ebenfalls im Fachjournal „Angewandte Chemie“ schildern die RUB-Forscher zusammen mit Kollegen der US-Universität in Salt-Lake City ein biobasiertes Verfahren für die Ammoniakproduktion. Die traditionelle Methode, um Ammoniak herzustellen, ist das Haber-Bosch-Verfahren – alt, bewährt, aber aufgrund des nötigen Drucks und der nötigen Temperatur sehr energieintensiv. Das Enzym Nitrogenase beherrscht ebenfalls den dazu nötigen Trick, um die außergewöhnlich starke Doppelbindung aufzubrechen, die zwischen zwei Stickstoffatomen besteht. Allerdings kann die Nitrogenase das bei Normaldruck und Raumtemperatur. Dazu benötigt sie jedoch ebenfalls für Zellen viel Energie in Form des Speichermoleküls ATP. Die Forscher haben nun auch hier mittels eines Redoxpolymers das Enzym fixiert und eine Verbindung zu einer Elektrode hergestellt, über die die nötige Reaktionsenergie von außen zugeführt werden kann. Damit hat das Team einen wichtigen Meilenstein erreicht, um die Bioelektrosynthese von Ammoniak durch Nitrogenasen zu ermöglichen.
bl