Enzym zur verbesserten CO2-Verwertung entdeckt
Ein Bremer Max-Planck-Team hat eine in Ölfeldern lebende Methan-Mikrobe untersucht, die CO2 elegant in Ameisensäure verwandeln kann.

Kohlendioxid aus Industrieprozessen nicht in die Atmosphäre zu entlassen, sondern chemisch aufzuwerten, dieser Ansatz soll einen kleinen Beitrag zur Klimaneutralität der Wirtschaft leisten. Gegenüber möglichen Ewigkeitsspeichern für CO2 ist das auch ökonomisch interessant, weil keine Entsorgungskosten anfallen, sondern sogar ein Gewinn erzielt werden kann. Dementsprechend intensiv wird an entsprechenden CO2-Nutzungsverfahren geforscht. Ein Team des Max-Planck-Instituts für Marine Mikrobiologie in Bremen hat nun einen besonders vielversprechenden Ansatz entdeckt und im Fachjournal "Angewandte Chemie" vorgestellt.
Archaee aus dem Umfeld von Ölfeldern
In der Natur gibt es einige Mikroorganismen, die CO2 aus der Luft fixieren und für ihren Stoffwechsel nutzen können. Unterschiedliche Forschungsgruppen haben in den vergangenen Jahren entsprechende Organismen identifiziert und teils darauf basierend biotechnologische Prozesse entwickelt. Das Bremer Team setzt auf die Archaee Methermicoccus shengliensis, eine Methan produzierende Mikrobe, die im Wasser um Tiefsee-Ölquellen lebt und sich bei Temperaturen von 65 Grad Celsius wohlfühlt.
Zunächst haben die Forschenden das Enzym identifiziert, das CO2 in Ameisensäure verwandelt. Ameisensäure ist für die chemische Industrie interessant, weil sie vielen chemischen Verbindungen als Ausgangsstoff dient und auch als Energiespeicher genutzt werden kann. „Wir wussten, dass solche Enzyme sauerstoffempfindlich sind. Deshalb mussten wir, um es von anderen Proteinen zu trennen, unter einer sauerstofffreien Haube ohne Umgebungsluft arbeiten – ziemlich kompliziert, aber es ist uns gelungen“, berichtet Olivier Lemaire.
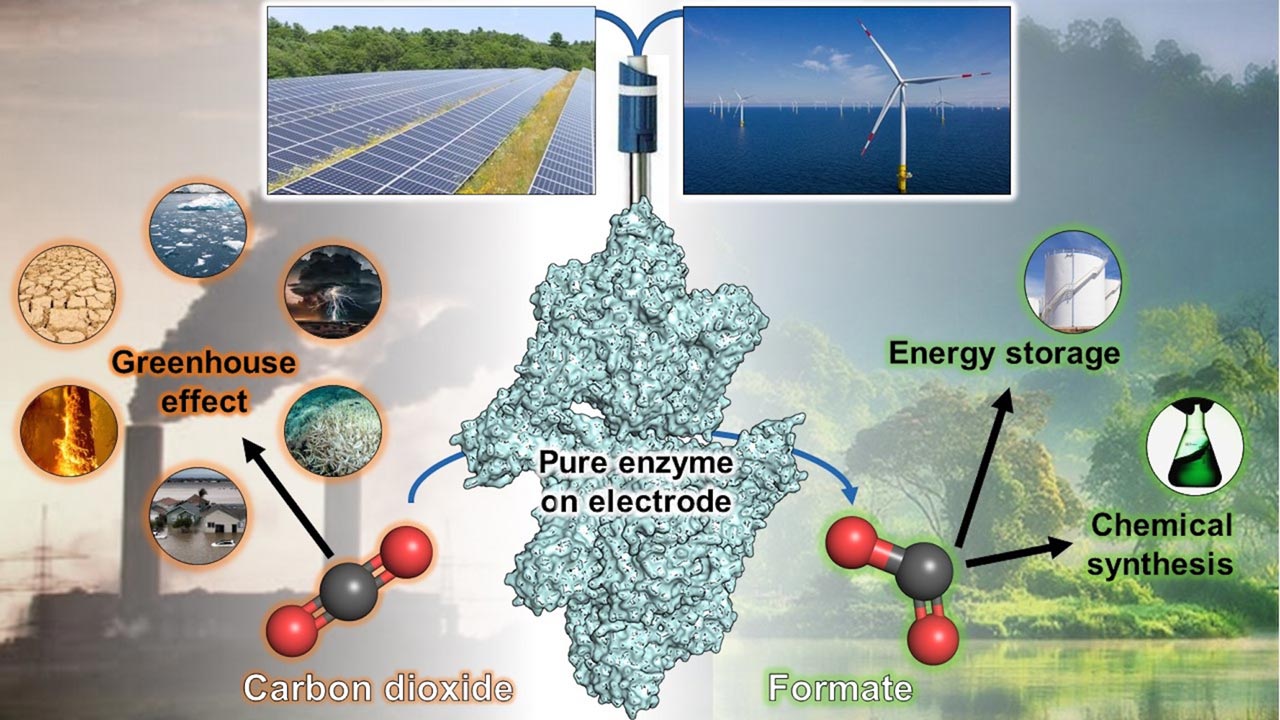
Enzyme setzt hauptsächlich die Hinreaktion um
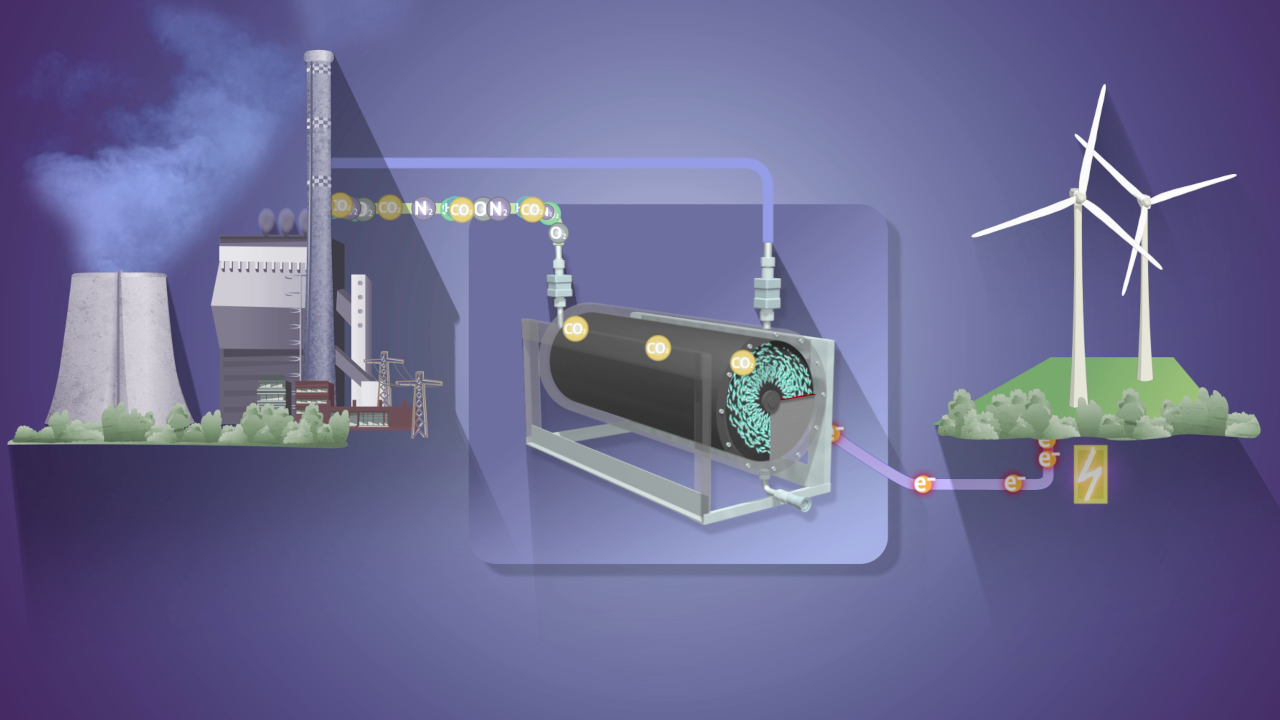
Schnell zeigte sich die Besonderheit des Enzyms: Anders als bei den Ameisensäure-Dehydrogenasen anderer Mikroorganismen erfolgt praktisch keine Rückreaktion von der Ameisensäure zum Kohlendioxid. „Dass die bei der CO2-Fixierung entstehende Ameisensäure nicht zurückverwandelt werden kann und sich daher anreichert, ist äußerst interessant für ein mögliches CO2-Abscheidungs-System, vor allem, wenn wir es auf einer Elektrode aufspannen könnten“, betont Tristan Wagner.
An eine Elektrode gebunden, könnte das Enzym seine benötigte Energie für die Umwandlungsreaktion aus dem Strom beziehen. Gegenüber anderen Energiequellen ist diese besonders günstig und führt zu effizienten Reaktionen. Und gegenüber der chemischen Synthese von Ameisensäure an einer Elektrode benötigt das Enzym keine giftigen Katalysatoren. Ein Team der Universität Genf hat deshalb die Herausforderung angenommen und mit diesem Enzym einen elektrobiotechnologischen Prozess entwickelt.
Reaktion ohne nachweisbare Nebenprodukte
Den Forschenden gelang es, das Enzym an eine Grafitelektrode zu koppeln. Die Rate, mit der das fixierte Enzym Kohlendioxid umwandelte, entsprach der anderer Ameisensäure-Dehydrogenasen. „Die Stärke dieses an die Elektrode gekoppelten biologischen Systems liegt darin, wie effizient es die Elektronen von der Elektrizität auf die CO2-Umwandlung überträgt“, betont Lemaire. Und auch in diesem System erfolgte praktisch keine Rückumwandlung der Ameisensäure. Stattdessen wandelte es kontinuierlich CO2 in Ameisensäure um, ohne dass dabei nachweisbare Nebenprodukte entstanden oder Strom verlorenging.
„Vor uns hat noch niemand versucht, ein Enzym von einer solchen methanogenen Mikrobe für eine elektrodenbasierte Gasumwandlung zu nutzen“, sagt Wagner. Dennoch sind noch viele prozesstechnische Probleme zu lösen, bis an eine großtechnisch Nutzung zu denken ist.
bl