Der Enzymarchitekt
Thomas HappeBeruf:
promovierter Biologe
Position:
Professor für Photobiotechnologie an der Ruhr-Universität Bochum

Beruf:
promovierter Biologe
Position:
Professor für Photobiotechnologie an der Ruhr-Universität Bochum

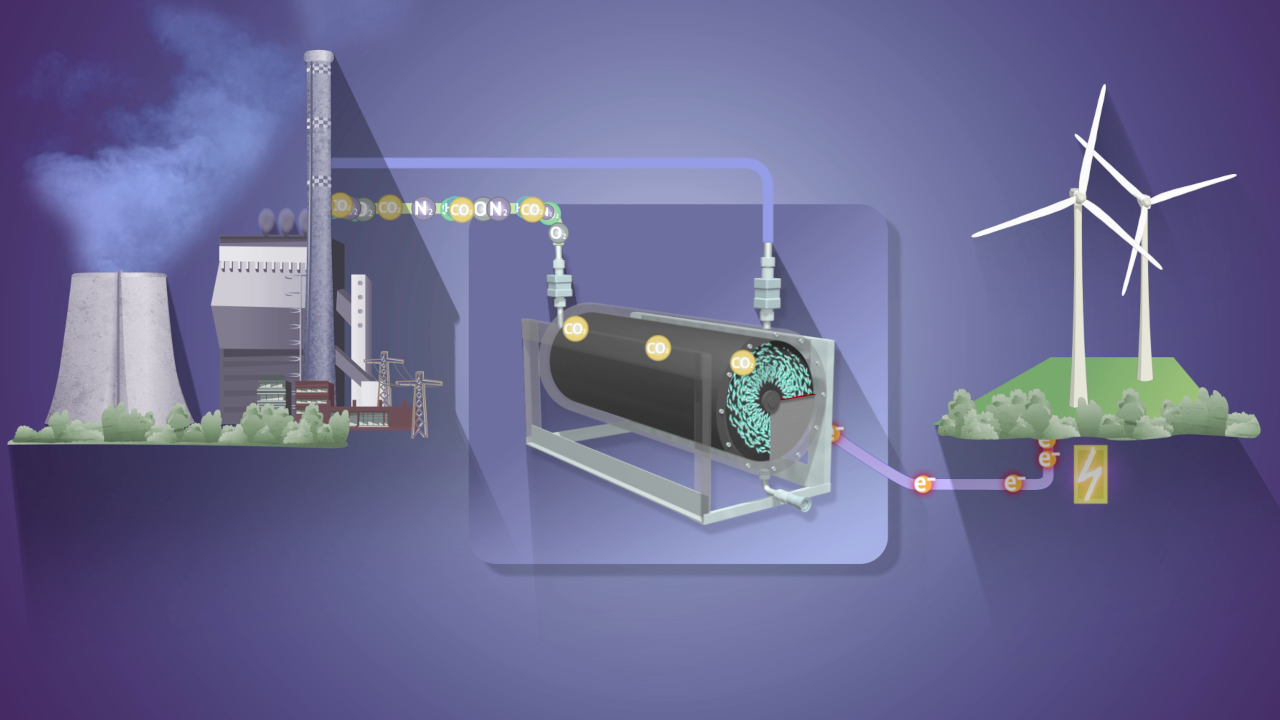
Der Photobiotechnologe Thomas Happe sucht nach neuartigen Strukturen, um regenerativ Wasserstoff herzustellen, wie es Algen können. Internationalität und Kooperation sieht der Forscher dabei als Schlüssel zum Erfolg.
Es ist ganz oft der Zufall, der eine Karriere in bestimmte Bahnen lenkt. Diese Erfahrung hat auch Thomas Happe vor vielen Jahren an der Ruhr-Universität Bochum gemacht. Als Biologiestudent traf er dort auf berühmte Photosyntheseforscher, unter ihnen der Pionier dieses Fachs, Achim Trebst, der mehr als vier Jahrzehnte die Forschung auf diesem Gebiet mitprägte und 2017 verstarb. Trebst fragte Happe seinerzeit, ob dieser nicht bei ihm promovieren wolle. Es war das erste Mal, dass der junge Mann mit Mikroalgen arbeitete und mit deren Enzym Hydrogenase, das für die Algen eine wichtige Rolle bei der Photosynthese spielt. Heute ist Happe selbst Professor für Photobiotechnologie an der Ruhr-Universität Bochum – und beschäftigt sich noch immer intensiv mit Algen und der Hydrogenase.
Aus der Arbeiterfamilie an die Uni
„Ich habe mich zwar schon als Kind für Biologie, für Natur interessiert, aber die Wege waren nicht vorherbestimmt“, erinnert sich Happe. Seine Überzeugung: „Man muss die richtigen Leute zur richtigen Zeit treffen und etwas Glück haben.“ Dass er studieren wollte, das hingegen stand für den Sohn einer Arbeiterfamilie aus dem Ruhrgebiet früh fest. Seinerzeit war das mit diesem Hintergrund kein einfacher Schritt. Heute freut es den Professor, dass es für junge Menschen in vergleichbaren Situationen vielfältige Unterstützung gibt.
Auch der Entschluss, das Biologiestudium für den Auftakt einer Forscherkarriere zu nutzen, reifte früh: „Über Achim Trebst bin ich in die Community reingerutscht, habe die Streitkultur in der Wissenschaft erlebt und wie sich neue Ideen entwickeln“, schildert der Forscher. „Das hat mich in seinen Bann gezogen – da wollte ich mitmachen.“ Begeistert habe ihn damals die Internationalität des Teams und die vielen Freiheiten, die ihm als junger Wissenschaftler gelassen wurden. „Damals habe ich auch die grünen Organismen lieben gelernt“, schmunzelt Happe.
Bei den Wasserstoffpionieren
Als Postdoc ging der Biotechnologe zunächst an die Universität Bonn, wurde dann von Anastasios Melis an die Universität Berkeley in Kalifornien eingeladen, wo beide gemeinsam an der Herstellung von Wasserstoff durch Algen forschten. „Die Hippiezeit war zwar vorbei, aber für mich war das eine exotische, interessante Stadt“, blickt Happe auf die Zeit mit San Francisco zurück. Aber auch das, was Melis und Happe vorhatten, erschien damals vielen seltsam und interessant zugleich.
Eine freie Professur an der Ruhr-Universität Bochum lockt den Forscher schließlich zurück in die Heimat. Hier pflegt er die Internationalität, die ihm schon früh gefallen hat. Man sieht sie an der Zusammensetzung seiner Arbeitsgruppe, aber auch an seinen Gastprofessuren in Australien und Japan. „Mein Interesse an anderen Kulturen versuche ich auch meinen Studenten weiterzugeben. Über das Erasmus-Programm haben sie heute viele Möglichkeiten.“
Der Biochemiker Thomas Happe benutzt Grünalgen als biologische Kraftwerke zur Herstellung von Brennstoffen oder Feinchemikalien.

An der Spitze der Hydrogenase-Forschung
Sein Team sieht Happe an der weltweiten Spitze der Hydrogenase-Forschung . Über sich selbst sagt er: „Ich bin Grundlagenforscher mit Ideen zur Anwendung – aber zuerst muss man die biologischen Mechanismen verstehen.“ Das sei faszinierend, oft aber auch sehr kompliziert. Das Interesse an seiner Arbeit erfährt Höhen und Tiefen. In der Klimawandel-Diskussion erlebe Wasserstoff gerade wieder eine große Aufmerksamkeit.
Was hat es denn nun auf sich mit der Hydrogenase? „Das Enzym kann in der Sekunde 10.000 Wasserstoffmoleküle herstellen, aber verträgt keinen Sauerstoff“, schildert Happe. Er sucht deshalb nach Möglichkeiten, das Enzym so zu verändern oder nachzubauen, dass Sauerstoff die Reaktion nicht länger stört. „Mein Alexander-Flemming-Experiment war, als wir einen chemisch synthetisierten Cofaktor mit einer Proteinhülle zusammenbrachten und so einen hoch effektiven biologischen Katalysator erhielten.“ Die technischen Möglichkeiten dazu habe es schon seit zwei Jahrzehnten gegeben, „aber es haben wohl alle bezweifelt, dass das klappen kann“, vermutet der Forscher, dem auch im eigenen Team zunächst Skepsis entgegenschlug. Mit diesem experimentellen Werkzeug standen Happe und seinem Team völlig neue Möglichkeiten offen, die biologische Wasserstoffbildung im atomaren Detail zu verstehen und sogar nachzubauen.
Stabile Alternativen zum ganzen Enzym
Künftig soll es genügen, anstelle der ganzen Proteinhülle nur bestimmte Aminosäuren dieser Hülle zu erzeugen und daran den für die Katalyse entscheidenden Cofaktor zu binden. „Dazu führen wir gezielte Änderungen auf atomarer Ebene ein und beobachten anhand der Kristallstrukturen, was das für die Katalyse bedeutet“, erklärt der Photobiotechnologe das Vorgehen. Das langfristige Ziel ist es, den Cofaktor an stabile, sauerstoffunempfindliche Strukturen zu binden.
Neben der Wasserstoffherstellung beschäftigt sich Happes Team auch mit weiteren Stoffen, die Algen produzieren können, beispielsweise für pharmazeutische Anwendungen. Ein interessantes Thema für Happe ist außerdem NADH, jenes Molekül, das als Elektronenträger biologische Reaktionen antreibt. Chemisch ist dessen Herstellung teuer, doch für biotechnologische Prozesse ist es oftmals unerlässlich. Gern würde Happe die Methoden der Zellen nachbilden, denen die NADH-Herstellung problemlos gelingt. Darüber hinaus wirkt die Gruppe des Forschers im Exzellenzcluster „Resolv“ mit, „das bietet viele Möglichkeiten, mit Chemikern vor Ort zu kooperieren“.
Im Labor von Thomas Happe ist eine wichtige Aufgabe das Screening nach neuartigen Enyzmen aus Mikroalgen.
Gemeinsam forscht sich‘s besser
Überhaupt: Neben der Internationalität ist Kooperation in den Augen Happes ein Schlüsselelement der Forschung. Es sei viel sinnvoller, ein teures Forschungsgerät, das man vielleicht nur zweimal im Monat benötigt, bei einem Kooperationspartner zu nutzen, als es selbst anzuschaffen. „Außerdem macht die Forschung gemeinsam viel mehr Spaß“, weiß der Bochumer. Das hat er während seines Sabbaticals belegt, das er gemeinsam mit seiner Familie in Australien und Japan verbrachte. Bei dortigen Forschungspartnern, die längst Freunde sind, hat er im Labor mitgewirkt und neue Ideen entwickelt, „frei von den täglichen Routinen einer Universität“, so Happe. „Im Kopf bin ich ständig bei meinem Beruf.“ Will er doch mal den Kopf frei bekommen, liest er gern, arbeitet im Garten, bewegt sich in der Natur bei ausgiebigen Spaziergängen oder nutzt dazu die Fahrradfahrt zwischen Wohnort und Universität.
Die Lehre schätzt der Professor trotzdem sehr. „Es freut mich, die Begeisterung in den Augen der jungen Leute zu sehen.“ Gerne begleite er junge Forscher, helfe und gebe Tipps. „Man spricht ja nicht umsonst vom Doktorvater.“ Nicht zuletzt böten die Vorlesungen Abwechslung: „Wenn die Forschung mal gerade schlecht läuft, freue ich mich umso mehr auf die Lehre“, schmunzelt Happe.
Neue Ansätze für die Zukunft
Für die Zukunft ist der Forscher voller Ideen. Erst kürzlich habe man gezeigt, dass die Biologie Wasserstoff anders zusammensetzt als der Chemiker. Letzterer fügt zunächst ein Elektron und ein Proton zu einem Wasserstoffatom zusammen, um dann mit viel Energieaufwand aus zwei Atomen ein Molekül zu formen. Die Natur allerdings erzeugt zunächst ein instabiles Hydridion aus zwei Elektronen und einem Proton, dem dann das zweite Proton hinzugefügt wird, um das Wasserstoffmolekül zu komplettieren. Das eröffnet ganz neue Forschungsansätze.
Natürlich weiß Happe, dass es von den Grundlagen bis zu einer Produktion im Großmaßstab ein weiter Weg ist. Dort warten neue Herausforderungen wie beispielsweise die, in einem großen Bioreaktor an alle Algenzellen genügend Licht zu leiten, ohne dass deren Stoffwechsel gestört wird. Daher arbeitet Happes Team auch daran, die Stoffwechselgrundlagen der Algen zu verstehen. Aber vor allem lockt den Forscher die Suche nach einfachen, günstigen Strukturen, auf die sich der Cofaktor der Hydrogenase übertragen lässt, und die man an Membranen binden kann, um so regenerativ Wasserstoff zu erzeugen. Aktuell untersucht sein Team, ob dazu nicht auch die chemisch sehr robuste DNA geeignet sein könnte. Bei der Produktionsmenge werden biologische Verfahren jedoch noch nicht mit chemischen Wasserstofffabriken konkurrieren können. „Mit unserem Wasserstoff werden Sie kein Auto antreiben, aber kleine Strukturen, beispielsweise Mikrobrennstoffzellen für Beleuchtungen.“
Darüber hinaus möchte Happe die Möglichkeiten der Algen bekannter machen. Dazu hat er 2015 das Start-up SolarBioproducts Ruhr mitgegründet. Es soll die Algenbiotechnologie vernetzen, aber auch durch Kochkurse und Wissenschaftsnächte in der Öffentlichkeit bekannter machen. Denn Algen können noch viel mehr als Wasserstoff herstellen.
Autor: Björn Lohmann