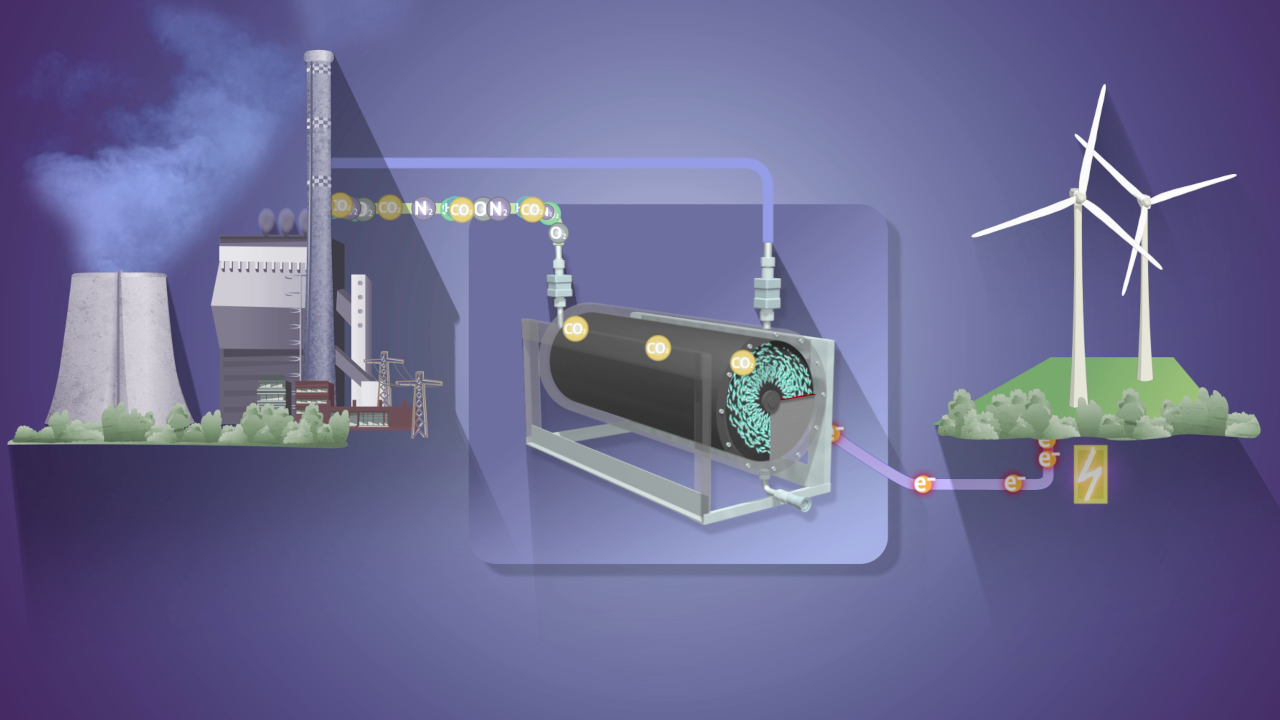
Die Biotechnologie ist längst kein junges Feld mehr, und doch entstehen immer wieder neue innovative Prozesse, die Aussicht auf eine Marktreife haben, für die aber noch keine industrielle Umsetzungsroutine existiert. Bioelektrochemische Prozesse gehören in diese Sparte neuer biobasierter Umsetzungen. Der Kern der mikrobiellen Bioelektrochemie ist die Interaktion von Mikroorganismen mit Elektroden. Einige Bakterien können mit Elektroden atmen: Elektronen, die bei der Produktion eines Wertstoffs anfallen, werden von diesen Organismen in der Atmung dann nicht auf Sauerstoff übertragen, sondern direkt an eine Elektrode weitergeleitet. Damit kann die Wertstoffproduktion mit einer Bereitstellung elektrischer Energie als Nebenprodukt gekoppelt werden. Aber lässt sich so ein Prozess industriell umsetzen und skalieren?
Kontinuierlicher Bioprozess für Acetoin
Die Antwort möchte das Forschungsprojekt „Conti-Bio-Elect“ liefern, das im Rahmen des Förderprogramms „Mikrobielle Biofabriken“ vom Bundesministerium für Bildung und Forschung unterstützt wird. Auf akademischer Seite erhalten das Engler-Bunte-Institut und das Institut für Angewandte Biowissenschaften am Karlsruher Institut für Technologie (KIT) zusammen rund 800.000 Euro. Seitens der Wirtschaft ist die Eisenhuth GmbH und Co. KG aus Osterode beteiligt. Das gemeinsame Ziel: einen kontinuierlich betriebenen Bioreaktor entwickeln, in dem das Proteobakterium Shewanella oneidensis aus Glukose Acetoin produziert und dazu auf einer Elektrode wächst, die anstelle von Sauerstoff die freiwerdenden Elektronen aufnimmt. Acetoin wird bislang zur Herstellung von Aromen vor allem chemisch synthetisiert und ist eine der 30 wichtigsten Plattformchemikalien.
„Anaerobe Bakterien erzeugen weniger Biomasse und haben potentiell höhere Produktausbeuten“, nennt Projektleiter Harald Horn vom KIT ein wichtiges Argument für das angestrebte kontinuierliche Verfahren. Denn anders als bei Batchverfahren wird hier der Reaktor nicht alle ein, zwei Tage komplett angehalten, gereinigt und wieder angefahren. Vielmehr sollen die Bakterien innerhalb des Reaktors für mehrere Wochen oder gar Monate fixiert an Oberflächen leben, das Substrat auf der einen Seite einströmen und das Produkt am anderen Ende entnommen werden – pausenlos. Das macht das kontinuierliche Verfahren wirtschaftlich sehr attraktiv, führt aber zu Problemen, wenn die Mikroorganismen sich zu schnell vermehren und neben dem Produkt auch überschüssige Biomasse ausgeschleust werden muss.
So sieht die montierte Fließzelle (links) und als Explosionszeichnung (rechts) aus, wie sie im Forschungsprojekt Conti-Bio-Elect genutzt wird.

Ein durchströmter Biofilter als Reaktormodell
„Bislang gibt es für unseren Zweck keine angepassten Reaktorsysteme“, erklärt Horn. „Wir selbst haben zwar Erfahrung mit solchen Biofilmreaktoren, aber die Aufwuchsflächen im Reaktor bestanden bislang nicht aus Elektroden.“ Eine Herausforderung wird daher darin bestehen, das geeignete Anodenmaterial zu identifizieren, auf dem der Mikroorganismus erfolgreich haftet und wächst. Die Anodenstruktur soll eine möglichst große Oberfläche bieten, um möglichst viele Bakterien beherbergen zu können. Als Reaktorvariante wurde ein aufwärts durchströmter Biofilter mit einer Schüttung aus Aufwuchsträgern in Form von Granulat gewählt. Nicht zuletzt muss dieses Granulat, aus dem die Anode bestehen soll, so dicht liegen, dass die Elektronen noch fließen können und für die Mikroorganismen das optimale elektrische Potenzial bieten. Dafür gilt es, Menge, Dichte und Porosität des Granulats zu optimieren. Im Blick hat das Forschungsteam dazu derzeit ein Polymer, das mit Graphit durchsetzt ist. Gelingt all das, können hohe Umsatzraten möglich sein.
Zunächst soll in einer kleinen Fließzelle getestet werden, welche Bedingungen und Materialien die besten Voraussetzungen bieten. Im Laufe des dreijährigen Projektzeitraums bis Ende Januar 2023 soll dann ein Prozess im 10- oder 20-Liter-Reaktor entstehen, der grundsätzlich auf industrielle Dimensionen hochskaliert werden kann. Darin könnte dann die Schüttung des Granulats aus mehreren unabhängigen Schichten bestehen, damit das geeignete Potenzial eingestellt werden kann. Bislang liegt das Teilprojekt zur Reaktorentwicklung trotz der Pandemie im Zeitplan.
Ein Gramm pro Liter und Stunde als Ziel
Schnell unterwegs ist auch das Team der Mikrobiologen im Projekt, denn S. oneidensis ist zwar von Natur aus elektroaktiv, muss aber für wirtschaftlich attraktive Stoffwechselraten in dieser Hinsicht genetisch optimiert werden. Mittels des Genomeditierungstools CRISPR/Cas soll das bewerkstelligt werden. Dabei kann die Arbeitsgruppe auf zehn Jahre Erfahrung mit demProteobakterium zurückgreifen. Bei den Tests in der Fließzelle soll der Erfolg überprüft werden: „Wie gut der Organismus auf der Anode wächst, sieht man“, erläutert Horn, „und wie produktiv er ist, erkennen wir am Stromfluss“ – mehr Elektronen bedeuten mehr Produktivität.
Wächst das Bakterium im Bioreaktor auch über längere Zeit und unter Hochlast, dann hofft das Forschungsteam auf eine ganz bestimmte Zahl: Produziert S. oneidensis mindestens ein Gramm Acetoin pro Liter und Stunde, „dann ist der Prozess wirtschaftlich attraktiv und wir haben unser Ziel erreicht“, sagt Horn mit Zuversicht.
Autor: Björn Lohmann