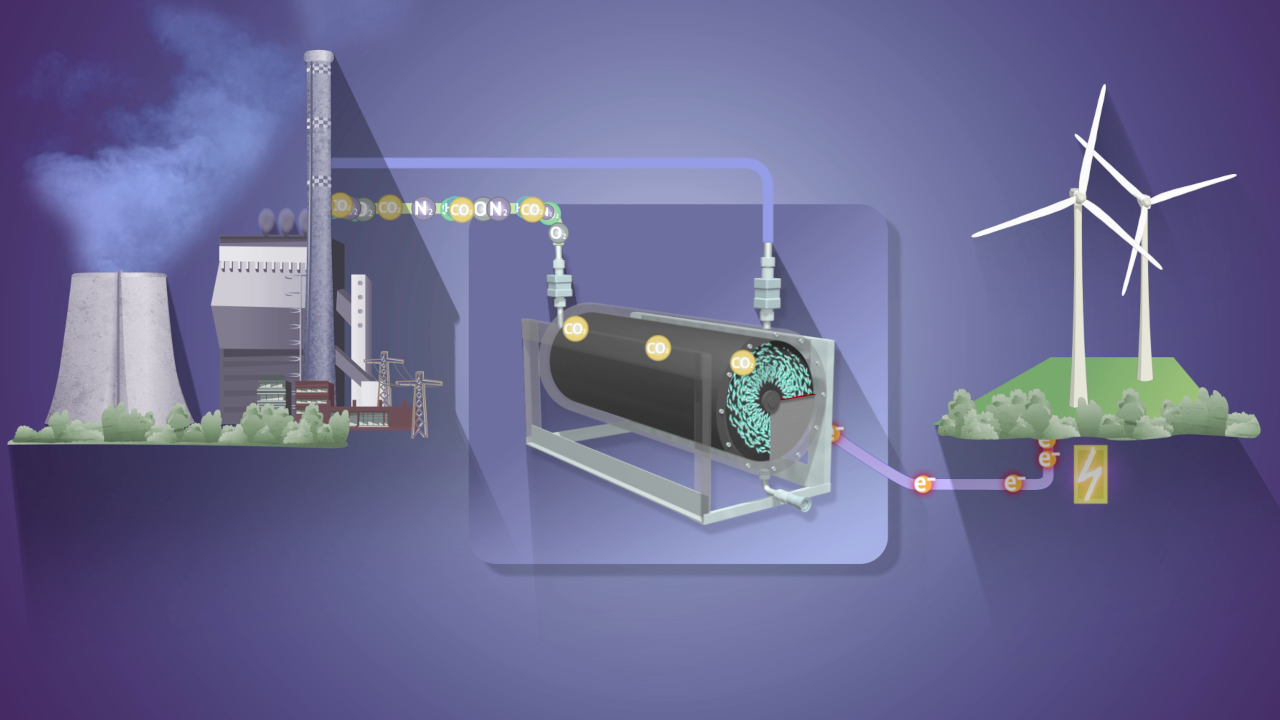
Stickstoff aus der Luft verwerten
Chemiker vom Leibniz-Institut für Katalyse in Rostock haben sich die Natur zum Vorbild genommen, um auf nachhaltige Weise Stickstoff aus der Luft nutzbar zu machen.

Knöllchenbakterien haben eine Fähigkeit, um die sie viele Chemiker beneiden: Die Mikroorganismen im Wurzelraum bestimmter Pflanzen können molekularen Stickstoff bei Normaltemperatur aufbrechen, um andere Moleküle herzustellen. Stickstoff liegt in der Atmosphäre elementar nur als Molekül aus zwei Atomen (N2) vor. Deren Elektronen bilden eine sogenannte Dreifachbindung, die äußerst stabil ist und das Molekül reaktionsträge macht. Mit roher Gewalt – Temperaturen bis 500 Grad Celsius und Drücken bis 350 Bar – machen Chemiker seit rund 100 Jahren das Molekül nutzbar. Chemiker des Leibniz-Instituts für Katalyse (LIKAT) in Rostock entwickeln dazu jetzt eine Alternative, die sich an der Chemie der Knöllchenbakterien orientiert.
Vorbild Knöllchenbakterien
In Knöllchenbakterien bindet ein Enzym namens Nitrogenase den elementaren Stickstoff und fungiert als Katalysator, um daraus Ammoniak (NH3) herzustellen. Das Enzym und diesen Prozess haben Mikrobiologen inzwischen gut verstanden. „In der Nitrogenase helfen Molybdän, teils auch Vanadium, und Eisen – also Metalle –, die Dreifachbindung des Luftstickstoffs aufzubrechen“, erläutert Nachwuchsgruppenleiter Christian Hering-Junghans vom LIKAT. Bereits 1995 hat er als Praktikant am MIT daran mitgewirkt, erstmalig ein Stickstoffmolekül bei Zimmertemperatur aufzubrechen und an ein Metall zu binden. Doch diese neue Bindung war so fest, dass sich der Stickstoff nicht weiter verwenden ließ.
Ein Korsett soll‘s richten
Jetzt soll der erneute Blick ins Knöllchenbakterium helfen. Dort werden die Metalle bei der Reaktion von einem festen molekularen Gerüst unterstützt. Genau so ein „Korsett“ hat Hering-Junghans mit seinem Team nun entwickelt. Im nächsten Schritt sollen die Metalle dort eingebettet werden. Mittels einer Kohlenstoffquelle wie Kohlendioxid könnte dann der Stickstoff vom Metall gelöst und an den Kohlenstoff gebunden werden. Verbindungen aus Stickstoff und Kohlenstoff sind in der chemischen Industrie stark nachgefragt. Deshalb will das Rostocker Team Luftstickstoff und CO2 für die Herstellung chemischer Grundstoffe nutzbar machen. Das Forschungsvorhaben mit dem Namen „LiDeNiAc“ (Ligand Design for Nitrogen Activation) wird von der EU bis 2020 im Rahmen des EU-Programms Horizon 2020 mit 168.000 Euro gefördert.
Großes Klimaschutzpotenzial
Eine Alternative zum Haber-Bosch-Verfahren wird auch aus Klimaschutzgründen dringend benötigt: Das Verfahren verursacht rund zwei Prozent des weltweiten gewerblichen Energiebedarfs. Jede Tonne auf diese Weise gewonnenes Ammoniak verursacht 1,5 Tonnen CO2-Emissionen. „Es lohnt sich also, zumindest jenen Teil der Ammoniakproduktion durch moderne Verfahren zu ersetzen, der nicht für die Pflanzendüngung gedacht ist“, betont Hering-Junghans.
bl